Hvilken base er den stærkeste i vandig opløsning?
Styrken af en base bestemmes af dens evne til at donere hydroxidioner (OH-) i vand. Jo stærkere basen er, jo flere hydroxidioner kan den donere.
I vandig opløsning er hydroxidion den stærkeste base, fordi den er den konjugerede base af vand, som er en meget svag syre. Det betyder, at hydroxidion er i stand til fuldstændigt at deprotonere vand og danne hydrogenioner (H+) og hydroxidioner.
Styrken af en base kan også udtrykkes i form af dens pKb-værdi, som er den negative logaritme af dens basisdissociationskonstant (Kb). Jo lavere pKb-værdi, jo stærkere basen.
pKb af hydroxidion er 0, hvilket betyder, at det er en meget stærk base. Dette skyldes, at hydroxidion er fuldstændig dissocieret i vand, hvilket betyder, at der ikke er nogen ligevægt mellem hydroxidion og vandmolekyler.
Andre stærke baser i vandig opløsning omfatter:
* Natriumhydroxid (NaOH)
* Kaliumhydroxid (KOH)
* Calciumhydroxid (Ca(OH)2)
* Bariumhydroxid (Ba(OH)2)
Disse baser er alle stærke, fordi de alle er i stand til at dissociere fuldstændigt i vand og danne hydroxidioner og de tilsvarende kationer.
Sidste artikelHvad er hydrogenoxidationstal?
Næste artikelHvad er nukleart brændsel lavet af?
 Varme artikler
Varme artikler
-
 Tubuli for at stoppe cellevækstDannelse og adskillelse af TOROIDer. Kredit:UNIGE TORC1 er et enzymkompleks, der styrer den normale vækst af celler. Imidlertid, når den er for aktiv, det kan fremme sygdomme som kræft. En undersø
Tubuli for at stoppe cellevækstDannelse og adskillelse af TOROIDer. Kredit:UNIGE TORC1 er et enzymkompleks, der styrer den normale vækst af celler. Imidlertid, når den er for aktiv, det kan fremme sygdomme som kræft. En undersø -
 Polymer-afledt kulstof som metalfrit, grønt alternativ til katalysatorer og nanocarbonerKredit:CC0 Public Domain Katalysatorer er nøglematerialer i det moderne samfund, muliggør selektiv omdannelse af råvarer til værdifulde produkter, samtidig med at spild reduceres og energi spares.
Polymer-afledt kulstof som metalfrit, grønt alternativ til katalysatorer og nanocarbonerKredit:CC0 Public Domain Katalysatorer er nøglematerialer i det moderne samfund, muliggør selektiv omdannelse af råvarer til værdifulde produkter, samtidig med at spild reduceres og energi spares. -
 Ikke sikker på, om du allerede har haft coronavirus? Denne test kan (måske) fortælle digMange mennesker spekulerer på, om den slemme forkølelse, de havde tilbage i februar eller marts, faktisk var den nye coronavirus. I princippet, en antistoftest kan fortælle dig, at men de fleste af te
Ikke sikker på, om du allerede har haft coronavirus? Denne test kan (måske) fortælle digMange mennesker spekulerer på, om den slemme forkølelse, de havde tilbage i februar eller marts, faktisk var den nye coronavirus. I princippet, en antistoftest kan fortælle dig, at men de fleste af te -
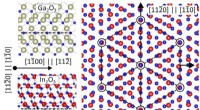 Ny katalytisk effekt fundet til fremstilling af galliumoxidMetaludvekslingskatalyse, som beskrevet, kan producere denne heterostruktur af galliumoxid-indiumoxid til ny elektronik baseret på galliumoxid. Kredit:PDI Halvledende oxider er en ny klasse af mat
Ny katalytisk effekt fundet til fremstilling af galliumoxidMetaludvekslingskatalyse, som beskrevet, kan producere denne heterostruktur af galliumoxid-indiumoxid til ny elektronik baseret på galliumoxid. Kredit:PDI Halvledende oxider er en ny klasse af mat
- En ny grafenkvantepunktstruktur tager kagen
- Unik undersøgelse tester grundlæggende fysiklove
- Forskere viser, hvordan calciumioner kan blokere natriumionkanaler i cellemembraner
- NASA vil sende mennesker til Venus - her er hvorfor det er en genial idé
- Tropiske cykloner kan forbedre mangroves sundhed
- Grizzly opdagelse af en pil gennem øjet kaster lys over forfærdelige skader forårsaget af middela…


