Hvilken type kemisk binding er oxygenfluorid?
 Varme artikler
Varme artikler
-
 Kemi-gennembrud åbner nye døre for lægemiddeludviklere og kræftforskereKugle-og-stok model af cubaner. Kredit:CC0 To uafhængige kemigennembrud har åbnet et væld af døre, der tidligere var låst for lægemiddeludviklere og kræftforskere. Opdagelserne, som involverede a
Kemi-gennembrud åbner nye døre for lægemiddeludviklere og kræftforskereKugle-og-stok model af cubaner. Kredit:CC0 To uafhængige kemigennembrud har åbnet et væld af døre, der tidligere var låst for lægemiddeludviklere og kræftforskere. Opdagelserne, som involverede a -
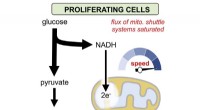 Sukkermetabolisme er overraskende konventionelt ved kræftGrafisk abstrakt. Kredit:Molecular Cell (2022). DOI:10.1016/j.molcel.2022.07.007 I over et århundrede har kræftcellernes stofskifte været betragtet som noget af et paradoks. Nyt arbejde fra forsker
Sukkermetabolisme er overraskende konventionelt ved kræftGrafisk abstrakt. Kredit:Molecular Cell (2022). DOI:10.1016/j.molcel.2022.07.007 I over et århundrede har kræftcellernes stofskifte været betragtet som noget af et paradoks. Nyt arbejde fra forsker -
 Gør som et blad:Forskere udvikler metode til at omdanne kuldioxidKredit:CC0 Public Domain Professor Jun Huang fra University of Sydneys School of Chemical and Biomolecular Engineering er ved at udvikle en kulstoffangstmetode, der sigter mod at gå et skridt ud o
Gør som et blad:Forskere udvikler metode til at omdanne kuldioxidKredit:CC0 Public Domain Professor Jun Huang fra University of Sydneys School of Chemical and Biomolecular Engineering er ved at udvikle en kulstoffangstmetode, der sigter mod at gå et skridt ud o -
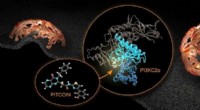 Inhibitor af lipidkinase PI3KC2a identificeret som potentiel ny behandling af tromboseKredit:Barth van Rossum Lipidkinasen PI3KC2a er et potentielt farmakologisk mål til behandling af trombose og muligvis cancer. Forskere fra Leibniz-Forschungsinstitut für Molekulare Pharmakologie (
Inhibitor af lipidkinase PI3KC2a identificeret som potentiel ny behandling af tromboseKredit:Barth van Rossum Lipidkinasen PI3KC2a er et potentielt farmakologisk mål til behandling af trombose og muligvis cancer. Forskere fra Leibniz-Forschungsinstitut für Molekulare Pharmakologie (
- Ny undersøgelse skitserer, hvorfor sydlige afrikansk-amerikanske skovejere mindre tilbøjelige til …
- Hvorfor har rekordstor regn i Japan været så dødbringende?
- Hvad er fremtiden for arbejde hjemmefra?
- Langsom transit af sediment i Australiens Murray-Darling flodsystem forvrænger miljøsignal:undersø…
- Edward C. Baig:Har du en god idé til 5G? Verizon kan give dig en million dollars for at få det til…
- Hvordan man tæller nanopartikler


