Kulstof skal danne fire kovalente bindinger for at fuldende sin ydre skal. Dette skyldes, at kulstof har fire valenselektroner, som er elektronerne i den yderste skal af et atom, der deltager i kemisk binding. Når carbonatomer binder sig til andre atomer, deler de deres valenselektroner for at opnå en stabil elektronkonfiguration. Kulstofatomer kan dele deres valenselektroner på en række forskellige måder, men den mest almindelige måde er at danne kovalente bindinger. I en kovalent binding deler to atomer et eller flere elektronpar. Når kulstof danner en kovalent binding, deler det en af dets valenselektroner med et andet atom, og det atom deler en af dets valenselektroner med kulstof. Dette skaber en stærk binding mellem de to atomer, og det giver kulstof mulighed for at opnå en stabil elektronkonfiguration.
 Varme artikler
Varme artikler
 Hvorfor bioelektroder til energiomdannelse ikke er stabileFelipe Conzuelo og Fangyuan Zhao har undersøgt, hvorfor kunstige fotosyntesesystemer er ustabile. Kredit:RUB, Kramer Forskere ved Ruhr-Universität Bochum har opdaget, hvorfor bioelektroder, der in
Hvorfor bioelektroder til energiomdannelse ikke er stabileFelipe Conzuelo og Fangyuan Zhao har undersøgt, hvorfor kunstige fotosyntesesystemer er ustabile. Kredit:RUB, Kramer Forskere ved Ruhr-Universität Bochum har opdaget, hvorfor bioelektroder, der in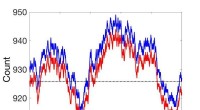 Ikke-steady state massehandlingsdynamik genovervejetSammenligninger mellem ikke-steady state stokastiske kinetiske simuleringer (rød) og simuleringer ved brug af koblet reaktionssætning (blå). Kredit:Pacific Northwest National Laboratory Masseaktio
Ikke-steady state massehandlingsdynamik genovervejetSammenligninger mellem ikke-steady state stokastiske kinetiske simuleringer (rød) og simuleringer ved brug af koblet reaktionssætning (blå). Kredit:Pacific Northwest National Laboratory Masseaktio Hurtigere, billigere spildevandsrensning gennem forbedrede oxidationsreaktionerUC Riverside-forskere har vist, at tilføjelse af en billig co-katalysator dramatisk kan forbedre hastigheden og effektiviteten af Advanced Oxidation Processes (AOPer). Kredit:UC Riverside Forske
Hurtigere, billigere spildevandsrensning gennem forbedrede oxidationsreaktionerUC Riverside-forskere har vist, at tilføjelse af en billig co-katalysator dramatisk kan forbedre hastigheden og effektiviteten af Advanced Oxidation Processes (AOPer). Kredit:UC Riverside Forske Bekæmpelse af lægemiddelresistens med hurtig, kunstig forstærkning af naturlige produkterForskere ved University of Tokyo bruger nye metoder til at imødegå den globale sundhedstrussel ved lægemiddelresistens og bygger nye antibiotika til at dræbe superbugen MRSA (methicillin-resistent Sta
Bekæmpelse af lægemiddelresistens med hurtig, kunstig forstærkning af naturlige produkterForskere ved University of Tokyo bruger nye metoder til at imødegå den globale sundhedstrussel ved lægemiddelresistens og bygger nye antibiotika til at dræbe superbugen MRSA (methicillin-resistent Sta

