Sammenlign stabiliteten af ammoniakkompleks versus en ethylendiamin med en metalion med koordinationsnummer 6, som højst sandsynligt ville reagere natriumhydroxidopløsning?
Generelt for en metalion med et koordinationstal på 6 er ethylendiaminkomplekser mere stabile end ammoniakkomplekser. Dette skyldes, at ethylendiamin er en bidentat ligand, hvilket betyder, at den kan donere to elektronpar til metalionen, mens ammoniak er en monodentat ligand og kun kan donere et elektronpar. Chelateffekten, som refererer til den øgede stabilitet af et kompleks med en multidentat ligand sammenlignet med et kompleks med multiple monodentate ligander, bidrager til den øgede stabilitet af ethylendiaminkomplekser.
Når man overvejer reaktionen af disse komplekser med natriumhydroxidopløsning, spiller ligandernes basicitet også en rolle. Ammoniak er en svagere base end ethylendiamin, hvilket betyder, at den er mindre tilbøjelig til at protonere i vandig opløsning. Som et resultat er ammoniakkomplekser mere tilbøjelige til at gennemgå ligandudvekslingsreaktioner med hydroxidioner fra natriumhydroxidopløsning, hvilket fører til dannelsen af metalhydroxidkomplekser.
I modsætning hertil er ethylendiamin en stærkere base, og dens komplekser er mindre tilbøjelige til at gennemgå ligandudvekslingsreaktioner med hydroxidioner. Derfor er ethylendiaminkomplekser generelt mere stabile i nærvær af natriumhydroxidopløsning sammenlignet med ammoniakkomplekser.
 Varme artikler
Varme artikler
-
 Forskere finder, at nogle ciderproducenter tilføjer unødvendigt sukkerKredit:CC0 Public Domain Det er feriesæsonen og den tid på året, hvor der er masser af libations ved næsten enhver begivenhed og eller fest. Imidlertid, du er muligvis ikke opmærksom på alle ingre
Forskere finder, at nogle ciderproducenter tilføjer unødvendigt sukkerKredit:CC0 Public Domain Det er feriesæsonen og den tid på året, hvor der er masser af libations ved næsten enhver begivenhed og eller fest. Imidlertid, du er muligvis ikke opmærksom på alle ingre -
 Gennembrud øger ydelsen af natrium-svovlbatterierVenstre til højre:Fremtrædende professor Shi Xue-Dou, Kære professor Huakun Liu, Lektor Shu-Lei Chou, Dr. Yunxiao Wang og hr. Zichao Yan fra Institute for Superconducting and Electronic Materials, Uni
Gennembrud øger ydelsen af natrium-svovlbatterierVenstre til højre:Fremtrædende professor Shi Xue-Dou, Kære professor Huakun Liu, Lektor Shu-Lei Chou, Dr. Yunxiao Wang og hr. Zichao Yan fra Institute for Superconducting and Electronic Materials, Uni -
 Forskere tager et nyt kig på Michaelis-Menten-ligningenMagnus Kjærgaard (til venstre) og Mateusz Dyla udfordrer en af hjørnestenene i biokemi, Michaelis-Menten-ligningen, da de viser, at mange enzymer i signalveje er uafhængige af substratkoncentration,
Forskere tager et nyt kig på Michaelis-Menten-ligningenMagnus Kjærgaard (til venstre) og Mateusz Dyla udfordrer en af hjørnestenene i biokemi, Michaelis-Menten-ligningen, da de viser, at mange enzymer i signalveje er uafhængige af substratkoncentration, -
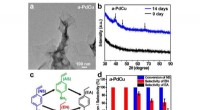 Heterofase nanostrukturer, der bidrager til effektiv katalyse(a) TEM-billede af a-PdCu nanoark. (b) XRD-mønstre af den som syntetiserede (0 dage) a-PdCu og a-PdCu efter ældning i 14 dage. (c) Hydrogeneringsreaktion af 4-nitrostyren (stuetemperatur, H2 ballon).
Heterofase nanostrukturer, der bidrager til effektiv katalyse(a) TEM-billede af a-PdCu nanoark. (b) XRD-mønstre af den som syntetiserede (0 dage) a-PdCu og a-PdCu efter ældning i 14 dage. (c) Hydrogeneringsreaktion af 4-nitrostyren (stuetemperatur, H2 ballon).
- Forbedring af ydeevnen af metal-organiske rammematerialer
- Et multishot-objektivløst kamera under udvikling kan hjælpe med at diagnosticere sygdom
- Billede:Nærbillede af neutronstjernemissioner røntgenkoncentratoroptik
- Billede:Jorden set fra 10, 000 miles
- Hvordan adskiller kulilte og dioxid sig?
- CES 2018:Google Smart Displays er 'vis og fortæl' svar på Echo Show


