Hvad indikerer -ate eller -ite i slutningen af en forbindelse?
1. Salte: I forbindelse med uorganisk kemi bruges -ate og -ite til at skelne mellem forskellige oxidationstilstande af et grundstof eller en forbindelse. -ate-suffikset angiver typisk en højere oxidationstilstand, mens -ite angiver en lavere oxidationstilstand. For eksempel:
- Sulfat (SO42-):højere oxidationstilstand af svovl (+6)
- Sulfit (SO32-):lavere oxidationstilstand for svovl (+4)
2. Estere og salte af syrer: I organisk kemi bruges -ate-suffikset til at angive en ester eller et salt af en organisk syre. -ite-suffikset bruges undertiden til estere eller salte af uorganiske syrer eller organiske syrer indeholdende svovl. For eksempel:
- Acetat:ester eller salt af eddikesyre
- Nitrit:salt af salpetersyrling
3. Mineraler: I mineralogi bruges suffikserne -ate og -ite til at skelne mellem forskellige mineraler baseret på deres sammensætning. For eksempel:
- Calcit (CaCO3):calciumcarbonatmineral
- Magnetit (Fe3O4):jernoxidmineral
4. Anioner og kationer: I uorganisk kemi kan -ate og -ite også bruges til at danne anioner og kationer. Anioner, der ender på -ate, kaldes anioner, mens dem, der ender på -ite, kaldes kationer. For eksempel:
- Sulfat (SO42-):anion
- Sulfit (SO32-):anion
- Nitrit (NO2-):anion
5. Funktionelle grupper: I organisk kemi kan -ate og -ite også bruges til at betegne forskellige funktionelle grupper. For eksempel:
- Carboxylat (-COO-):carboxylatfunktionel gruppe
- Sulfit (-SO3-):sulfitfunktionel gruppe
Det er vigtigt at bemærke, at den specifikke betydning af -ate og -ite kan variere afhængigt af det pågældende felt og forbindelse.
Sidste artikelHvad gør nogle grundstoffer til ioner?
Næste artikelKan nikkel reagere med saltsyre?
 Varme artikler
Varme artikler
-
 Svampeenzymer kan holde hemmeligheden bag fremstillingen af vedvarende energi fra træEn overordnet tredimensionel struktur af en af denne klasse af enzymer. Kredit:Professor Gideon Davies, University of York Et internationalt team af forskere, inklusive videnskabsmænd fra Univer
Svampeenzymer kan holde hemmeligheden bag fremstillingen af vedvarende energi fra træEn overordnet tredimensionel struktur af en af denne klasse af enzymer. Kredit:Professor Gideon Davies, University of York Et internationalt team af forskere, inklusive videnskabsmænd fra Univer -
 Biosensor muliggør iltovervågning i realtid for organer-på-en-chipEn ny biosensor giver forskere mulighed for at spore iltniveauer i realtid i organ-on-a-chip-systemer, gør det muligt at sikre, at sådanne systemer i højere grad efterligner virkelige organers funktio
Biosensor muliggør iltovervågning i realtid for organer-på-en-chipEn ny biosensor giver forskere mulighed for at spore iltniveauer i realtid i organ-on-a-chip-systemer, gør det muligt at sikre, at sådanne systemer i højere grad efterligner virkelige organers funktio -
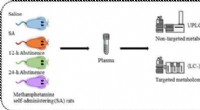 En rottehjerne, til og fra metamfetaminKredit:American Chemical Society Stofmisbrug er en ond cirkel af belønning og tilbagetrækning. Kroniske brugere får ofte tilbagefald på grund af de ubehagelige fysiske og psykiske symptomer, de op
En rottehjerne, til og fra metamfetaminKredit:American Chemical Society Stofmisbrug er en ond cirkel af belønning og tilbagetrækning. Kroniske brugere får ofte tilbagefald på grund af de ubehagelige fysiske og psykiske symptomer, de op -
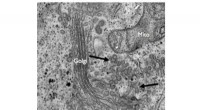 Enzym har vist sig at kontrollere dannelsen af kollagenbærere og hæmme kollagensekretionElektronmikroskopi-billeddannelse afslører tilstedeværelsen af mange indbyrdes forbundne vesikler, som ser ud til at opføre sig som kollagenbærere (angivet med pile). Kredit: Biokemisk og biofysisk
Enzym har vist sig at kontrollere dannelsen af kollagenbærere og hæmme kollagensekretionElektronmikroskopi-billeddannelse afslører tilstedeværelsen af mange indbyrdes forbundne vesikler, som ser ud til at opføre sig som kollagenbærere (angivet med pile). Kredit: Biokemisk og biofysisk
- Forskere indsnævrer søgningen efter mørke fotoner ved hjælp af årti gamle partikelkolliderdata
- Instruktioner til et Egg Drop Science Fair-projekt
- Ny NASA-mission vil studere ultraviolet himmel, stjerner, stjerneeksplosioner
- Forskere leder efter begyndelsen af menneskelig informationsdeling
- Hvad er kationnavnet for NaO2?
- Kan kapitalismen og planeten virkelig eksistere side om side?


