Hvorfor er mange forbindelser, der indeholder et- eller malmbrinteatomer, ikke klassificeret som Arrhenius-syre?
Ifølge Arrhenius definition af syrer betragtes et stof som en syre, hvis det dissocierer i vand for at producere hydrogenioner (H+). Denne definition understreger i høj grad ioniseringsprocessen og tilstedeværelsen af frie H+ ioner i opløsningen.
Mange forbindelser, der indeholder brintatomer, gennemgår ikke ionisering i vand. Det betyder, at de ikke frigiver H+-ioner, når de er opløst, og derfor opfylder de ikke kriterierne for at blive klassificeret som Arrhenius-syrer. For eksempel:
1. Hydrocarboner: Kulbrinter, såsom methan (CH4) eller benzen (C6H6), er udelukkende sammensat af kulstof- og brintatomer. De ioniserer dog ikke i vand og frigiver ikke H+ ioner. De betragtes således ikke som Arrhenius-syrer.
2. Alkoholer: Alkoholer, såsom ethanol (CH3CH2OH), indeholder både carbon-hydrogen-bindinger og en -OH (hydroxyl) gruppe. På trods af at de har et hydrogenatom bundet til et oxygenatom, gennemgår alkoholer meget begrænset ionisering i vand. -OH-gruppen frigiver en proton (H+) i meget lille udstrækning og danner hydroniumioner (H3O+). Omfanget af ionisering er dog ubetydeligt sammenlignet med stærke syrer. Derfor er alkoholer ikke klassificeret som Arrhenius-syrer.
3. Ammoniak (NH3): Ammoniak er en forbindelse af nitrogen og brint. Det opfører sig dog som en base i stedet for en syre i vand. Når det opløses i vand, gennemgår ammoniak en reaktion kaldet protonering, hvor det accepterer en proton fra vand og danner ammoniumioner (NH4+) og hydroxidioner (OH-). Derfor er ammoniak ikke en Arrhenius-syre.
I modsætning hertil klassificeres forbindelser som saltsyre (HCl), svovlsyre (H2SO4) eller salpetersyre (HNO3) som Arrhenius-syrer, fordi de let dissocieres i vand og frigiver betydelige mængder hydrogenioner.
Sammenfattende, mens mange forbindelser indeholder brintatomer, er det kun dem, der undergår ionisering i vand og frigiver hydrogenioner (H+), der klassificeres som Arrhenius-syrer ifølge den strenge definition. Forbindelser, der ikke ioniserer i væsentlig grad, såsom kulbrinter, alkoholer eller ammoniak, betragtes ikke som Arrhenius-syrer.
 Varme artikler
Varme artikler
-
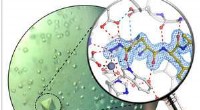 En kemisk skræddersyet dragt til Alzheimers medicinProteinkrystaller af det humane enzym glutaminylcyclase og atomstruktur af den nye inhibitor. Kredit:Lisa-Marie Funk Med over 1,2 millioner mennesker berørt alene i Tyskland og over 50 millioner m
En kemisk skræddersyet dragt til Alzheimers medicinProteinkrystaller af det humane enzym glutaminylcyclase og atomstruktur af den nye inhibitor. Kredit:Lisa-Marie Funk Med over 1,2 millioner mennesker berørt alene i Tyskland og over 50 millioner m -
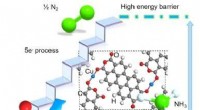 En ny strategi for elektrokemisk reduktion af nitrat til ammoniakForeslået struktur af Cu-inkorporeret PTCDA og skematisk diagram, der illustrerer dens fordel ved selektivt at reducere NO3− til NH3 via direkte 8-eletron overførsel. Rød, hvid, grå, strålende blå, og
En ny strategi for elektrokemisk reduktion af nitrat til ammoniakForeslået struktur af Cu-inkorporeret PTCDA og skematisk diagram, der illustrerer dens fordel ved selektivt at reducere NO3− til NH3 via direkte 8-eletron overførsel. Rød, hvid, grå, strålende blå, og -
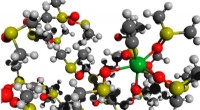 En ny strategi for grønnere anvendelse af calciumcarbidBorn-Oppenheimer molekylær dynamik af et acetylidmolekyle HO-Ca-CCH solvatiseret i DMSO. Kredit:Mikhail Polynski, assistentlærer ved Institute of Chemistry ved St Petersburg University Calciumacet
En ny strategi for grønnere anvendelse af calciumcarbidBorn-Oppenheimer molekylær dynamik af et acetylidmolekyle HO-Ca-CCH solvatiseret i DMSO. Kredit:Mikhail Polynski, assistentlærer ved Institute of Chemistry ved St Petersburg University Calciumacet -
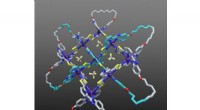 Forskere opdager en ny type molekylær knude ved hjælp af røntgendiffraktionsteknikkerDavid Leigh, University of Manchester. Forskere har udviklet en måde at flette tre molekylære tråde, så det er muligt at lave strammere og mere komplekse knuder, end det tidligere har været muligt
Forskere opdager en ny type molekylær knude ved hjælp af røntgendiffraktionsteknikkerDavid Leigh, University of Manchester. Forskere har udviklet en måde at flette tre molekylære tråde, så det er muligt at lave strammere og mere komplekse knuder, end det tidligere har været muligt
- Hvilket udsagn om den første optræden af organismer over en tidsperiode, der er repræsenteret i…
- Hvad er det næste for Siemens og Alstom efter fusionsveto?
- Effekten af Mars ionosfæriske spredning på SAR-billeddannelse
- Flere grunde til optimisme med hensyn til klimaændringer, end vi har set i årtier
- Lab demonstrerer med succes ny teknik til at forbedre partikelstråler
- Forskerhold bekræfter, at der var iskolde forhold i Sydpol-regionen under den sene kridtperiode


