Hvad er en skal i kemi?
Skallerne er betegnet med bogstaver, startende med den inderste skal mærket som "K", efterfulgt af "L", "M", "N" og så videre, når vi bevæger os længere væk fra kernen. Hver skal kan indeholde et bestemt antal elektroner. Det maksimale antal elektroner, som en skal kan indeholde, bestemmes af formlen 2n², hvor "n" er antallet af skallen.
For eksempel:
- K-skallen (n =1) kan maksimalt rumme 2(1)² =2 elektroner.
- L-skallen (n =2) kan maksimalt rumme 2(2)² =8 elektroner.
- M-skallen (n =3) kan maksimalt rumme 2(3)² =18 elektroner.
Når vi bevæger os til højere skaller, stiger energiniveauet, og elektronerne oplever en svagere tiltrækning til kernen. Fyldningen af elektronskaller følger visse regler og mønstre og bestemmer den elektroniske konfiguration af atomer, som spiller en afgørende rolle i forståelsen af deres kemiske egenskaber og adfærd.
 Varme artikler
Varme artikler
-
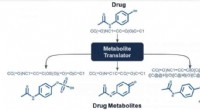 Dyb læring giver lægemiddeldesign et løftEt beregningsværktøj skabt på Rice University kan hjælpe medicinalvirksomheder med at udvide deres evne til at undersøge lægemidlers sikkerhed. Kredit:Kavraki Lab/Rice University Når du tager medi
Dyb læring giver lægemiddeldesign et løftEt beregningsværktøj skabt på Rice University kan hjælpe medicinalvirksomheder med at udvide deres evne til at undersøge lægemidlers sikkerhed. Kredit:Kavraki Lab/Rice University Når du tager medi -
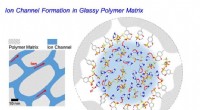 Vil stærk og hurtigt skiftende kunstig muskel være mulig?Skematisk diagram af ionkanaldannelse inde i polymerelektrolytten. Kredit:POSTECH I den amerikanske actionfilm Pacific Rim kæmper gigantiske robotter kaldet Jaegers mod ukendte monstre for at redde
Vil stærk og hurtigt skiftende kunstig muskel være mulig?Skematisk diagram af ionkanaldannelse inde i polymerelektrolytten. Kredit:POSTECH I den amerikanske actionfilm Pacific Rim kæmper gigantiske robotter kaldet Jaegers mod ukendte monstre for at redde -
 Opbygning af stivelsesrygrad til laboratoriedyrket kød ved hjælp af lego-stykkerEn elektrospinner lavet af lego-stykker bruges til at lave stivelsestråde. Kredit:Patrick Mansell En ny teknik til at spinde stivelsesfibre ved hjælp af lego-stykker kan have fremtidige anvendelse
Opbygning af stivelsesrygrad til laboratoriedyrket kød ved hjælp af lego-stykkerEn elektrospinner lavet af lego-stykker bruges til at lave stivelsestråde. Kredit:Patrick Mansell En ny teknik til at spinde stivelsesfibre ved hjælp af lego-stykker kan have fremtidige anvendelse -
 Support driver skæbnen for beskyttede guld-nanoklynger som katalysatorerForskningen blev lavet på forsiden af Chemistry-A European Journal i juni 2020. På billedet:guldklynger (gule ædelstene) beskyttet af organiske molekyler (lyserøde og blå ædelstene) opdeles på to fo
Support driver skæbnen for beskyttede guld-nanoklynger som katalysatorerForskningen blev lavet på forsiden af Chemistry-A European Journal i juni 2020. På billedet:guldklynger (gule ædelstene) beskyttet af organiske molekyler (lyserøde og blå ædelstene) opdeles på to fo
- En lomme fuld af vandmolekyler - hvordan aktinfilamenter driver cellens bevægelse
- At finde ny kemi til at fange det dobbelte kulstof
- Nye sanseteknikker kan detektere tørketolerance i gamle afgrøder, kan informere nye avlsprogrammer…
- Kan nuklear produktion reducere europæisk afhængighed af russisk gas?
- Små satellitter giver store kommercielle muligheder
- Forskere skaber niende måde at dræbe et batteri på


