Hvad er en gruppe af grundstoffer i det periodiske system?
Det periodiske system er arrangeret således, at grundstofferne i hver gruppe har lignende kemiske egenskaber. For eksempel er alle alkalimetallerne (gruppe 1) meget reaktive og har en valenselektron. Alle halogenerne (gruppe 7) er meget reaktive og har syv valenselektroner.
Grupperne i det periodiske system er nummereret 1-18 fra venstre mod højre. Grupperne er også opdelt i to kategorier:hovedgruppeelementer og overgangsmetaller. Hovedgruppeelementerne er elementerne i gruppe 1, 2, 13-18. Overgangsmetallerne er grundstofferne i gruppe 3-12.
Hovedgruppeelementerne er yderligere opdelt i tre kategorier:metaller, ikke-metaller og metalloider. Metaller er elementer, der er skinnende, formbare og duktile. Ikke-metaller er elementer, der ikke er skinnende, ikke er formbare eller duktile og er dårlige ledere af varme og elektricitet. Metalloider er grundstoffer, der har egenskaber af både metaller og ikke-metaller.
Overgangsmetallerne er alle metaller, men de har en bredere vifte af egenskaber end hovedgruppens metaller. Overgangsmetaller er generelt hårde, stærke og har høje smeltepunkter. De er også gode ledere af varme og elektricitet.
Det periodiske system er et værdifuldt værktøj til at forstå grundstoffernes egenskaber, og hvordan de interagerer med hinanden. Ved at forstå grupperne og kategorierne af elementer kan du bedre forstå stoffets adfærd.
Sidste artikelIndeholder CCL4 kovalente og ioniske forbindelser?
Næste artikelHvad er argons reaktivitet med ilt?
 Varme artikler
Varme artikler
-
 Vigtige trin til transformation af giftige molekyler i luft ved lave temperaturerBiludstødningsluftforurening i byer. Novosibirsk, vinter 2021. Kredit:S. Dukhovnikov Luftforurening fra brændstofforbrænding er et af de største miljøproblemer, især i bymiljøer. I tæt befolkede b
Vigtige trin til transformation af giftige molekyler i luft ved lave temperaturerBiludstødningsluftforurening i byer. Novosibirsk, vinter 2021. Kredit:S. Dukhovnikov Luftforurening fra brændstofforbrænding er et af de største miljøproblemer, især i bymiljøer. I tæt befolkede b -
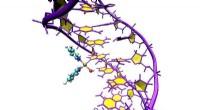 Hvordan interagerer metaller med DNA?Computersimuleringer viser den præcise placering af Pt103 i DNA. Kredit:Juan J. Nogueira, Universitetet i Wien I et par årtier, metalholdige lægemidler er med succes blevet brugt til at bekæmpe vi
Hvordan interagerer metaller med DNA?Computersimuleringer viser den præcise placering af Pt103 i DNA. Kredit:Juan J. Nogueira, Universitetet i Wien I et par årtier, metalholdige lægemidler er med succes blevet brugt til at bekæmpe vi -
 Dyrkning af metallisk træ til nye højderDenne strimmel af metallisk træ, omkring en tomme lang og en tredjedel tomme bred, er tyndere end husholdnings-aluminiumsfolie, men bærer mere end 50 gange sin egen vægt uden at knække. Hvis vægten bl
Dyrkning af metallisk træ til nye højderDenne strimmel af metallisk træ, omkring en tomme lang og en tredjedel tomme bred, er tyndere end husholdnings-aluminiumsfolie, men bærer mere end 50 gange sin egen vægt uden at knække. Hvis vægten bl -
 Opbevar håndværksøl på et køligt sted og spis det så frisk som muligtBilledet viser humlekogler. Kredit:Dr. Martin Steinhaus En ny undersøgelse foretaget af Leibniz-Institute for Food Systems Biology ved det tekniske universitet i München (Leibniz-LSB@TUM) viser, a
Opbevar håndværksøl på et køligt sted og spis det så frisk som muligtBilledet viser humlekogler. Kredit:Dr. Martin Steinhaus En ny undersøgelse foretaget af Leibniz-Institute for Food Systems Biology ved det tekniske universitet i München (Leibniz-LSB@TUM) viser, a
- Forskere bruger en blender til at afsløre, hvad der er i vores smartphones
- Maxwells ligninger: Definition, derivation, hvordan man kan huske (w /eksempler)
- Hvad har Twitter med den menneskelige hjerne at gøre?
- Nordøstbønder vejer det opvarmende klima, gennemblødte marker
- Forbindelsen mellem kød og social status
- Sproget kan underminere kvinder inden for videnskab og teknologi


