En opløsning af HBr har H plus er lig med 2,1 x 10-6 Hvad er pH i denne opløsning?
$$pH =-\log_{10}[H+]$$
Givet at [H+] =2,1 x 10-6 M, kan vi erstatte denne værdi i ligningen:
$$pH =-\log_{10}(2,1 \times 10^{-6})$$
$$pH =5,68$$
Derfor er pH-værdien af HBr-opløsningen ca. 5,68.
 Varme artikler
Varme artikler
-
 Bakterielt enzym ekstraherer sjældne jordarters elementer på en miljøvenlig mådeSjældne jordarters grundstoffer fra Lanthanum (La) til Europium (Eu). Med stigende atomvægt, ionradius falder sekventielt. Kredit:imago images / JOKER / Alexander Stein Sjældne jordarters elemente
Bakterielt enzym ekstraherer sjældne jordarters elementer på en miljøvenlig mådeSjældne jordarters grundstoffer fra Lanthanum (La) til Europium (Eu). Med stigende atomvægt, ionradius falder sekventielt. Kredit:imago images / JOKER / Alexander Stein Sjældne jordarters elemente -
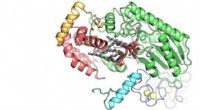 Forskere kortlægger vigtige immunsystemenzym for første gangKrystalstruktur af værtsenzymet, Acyloxyacylhydrolase (AOAH), i kompleks med lipopolysaccharid (LPS) vist med grå pinde, som er et potent bakterietoksin. Figuren viser en af de seks fedtsyrekæder af
Forskere kortlægger vigtige immunsystemenzym for første gangKrystalstruktur af værtsenzymet, Acyloxyacylhydrolase (AOAH), i kompleks med lipopolysaccharid (LPS) vist med grå pinde, som er et potent bakterietoksin. Figuren viser en af de seks fedtsyrekæder af -
 Teknik kan gøre det lettere at bruge mRNA til at behandle sygdom eller levere vacciner”Hvis vi vil være i stand til at levere mRNA, så har vi brug for en mekanisme til at være mere effektiv til det, fordi alt, hvad der har været brugt indtil nu, giver dig en meget lille brøkdel af, hva
Teknik kan gøre det lettere at bruge mRNA til at behandle sygdom eller levere vacciner”Hvis vi vil være i stand til at levere mRNA, så har vi brug for en mekanisme til at være mere effektiv til det, fordi alt, hvad der har været brugt indtil nu, giver dig en meget lille brøkdel af, hva -
 Klimatilbagespoling:Forskere omdanner kuldioxid tilbage til kulEn skematisk illustration, der viser, hvordan flydende metal bruges som katalysator til at omdanne kuldioxid til fast kul. Kredit:RMIT University Forskere har brugt flydende metaller til at omdann
Klimatilbagespoling:Forskere omdanner kuldioxid tilbage til kulEn skematisk illustration, der viser, hvordan flydende metal bruges som katalysator til at omdanne kuldioxid til fast kul. Kredit:RMIT University Forskere har brugt flydende metaller til at omdann
- Spøgelsespartikel ML-model tillader fuld kvantebeskrivelse af den solvatiserede elektron
- AI-værktøjer afslører mangel på ikke-hvide, ikke-mandlige karakterer i almindelige bøger
- En ny sphenodontian fra Brasilien er den ældste rekord for gruppen i Gondwana
- Fire måder at fremskynde en kemisk reaktion
- Hawaii vulkan sender lava boblende, styrker 1, 500 fra hjemmet
- Uvis klimafremtid kan forstyrre energisystemerne


