Hvad sker der, når syre tilsættes forskellige metaller?
1. Aktive metaller:
- Aktive metaller, såsom natrium, kalium og calcium, reagerer kraftigt med syrer.
- Reaktionen producerer brintgas, varme og et salt sammensat af metallet og anionerne fra syren.
- For eksempel, når saltsyre (HCl) reagerer med natriummetal (Na), producerer den hydrogengas (H2), varme og natriumchlorid (NaCl).
2. Mindre aktive metaller:
- Mindre aktive metaller, såsom jern, zink og magnesium, reagerer langsomt med syrer.
- Reaktionen producerer brintgas, varme og et salt.
- Reaktionen kan dog kræve opvarmning eller en stærkere syre for nogle mindre aktive metaller.
3. Ikke-reaktive metaller:
- Ædelmetaller, såsom guld, sølv og platin, er generelt ikke-reaktive over for syrer.
- Disse metaller reagerer ikke eller reagerer meget langsomt med de fleste syrer.
4. Syrestyrke:
- Syrens styrke påvirker også reaktiviteten. Stærkere syrer, såsom saltsyre (HCl) og svovlsyre (H2SO4), reagerer kraftigere end svagere syrer, såsom eddikesyre (CH3COOH).
5. Saltdannelse:
- I alle tilfælde, hvor der opstår en reaktion, er produktet et salt. Saltet er sammensat af metalkationen og anionen fra syren.
6. Brintgasproduktion:
- Reaktionen mellem metaller og syrer giver brintgas. Mængden af produceret brint afhænger af mængden af metal og syrens styrke.
7. Potentielle farer:
- Reaktioner mellem syrer og metaller kan være farlige på grund af frigivelse af brændbar brintgas og varme. Korrekte sikkerhedsforanstaltninger, såsom at arbejde i et godt ventileret område og bære beskyttelsesudstyr, er afgørende ved håndtering af syrer og metaller.
Det er vigtigt at bemærke, at disse er generelle observationer, og den specifikke reaktivitet af et metal med en syre kan variere afhængigt af det nøjagtige metal og den involverede syre.
Sidste artikelHvilket molekylært fast stof ville have den højeste smeltning?
Næste artikelEr en snemand kemisk forandring?
 Varme artikler
Varme artikler
-
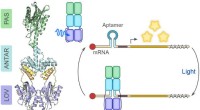 Blåt lys til RNA -kontrolFotoreceptoren PAL binder korte ribonukleinsyrer ved bestråling af blåt lys. Denne lysstyrede aktivitet kan bruges til at regulere RNA-baserede processer, såsom translation. Kredit:© Andreas Möglich/U
Blåt lys til RNA -kontrolFotoreceptoren PAL binder korte ribonukleinsyrer ved bestråling af blåt lys. Denne lysstyrede aktivitet kan bruges til at regulere RNA-baserede processer, såsom translation. Kredit:© Andreas Möglich/U -
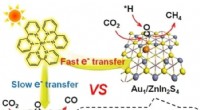 Enkelte guldatomer katalyserer den selektive metanisering af kuldioxidKredit:Wiley Et skridt mod kuldioxid (CO2 ) neutralitet og afbødning af både drivhuseffekten og energikrisen ville være at omdanne CO2 til kulbrintebaserede brændstoffer som metan ved hjælp af lys.
Enkelte guldatomer katalyserer den selektive metanisering af kuldioxidKredit:Wiley Et skridt mod kuldioxid (CO2 ) neutralitet og afbødning af både drivhuseffekten og energikrisen ville være at omdanne CO2 til kulbrintebaserede brændstoffer som metan ved hjælp af lys. -
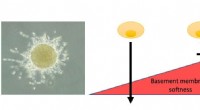 Ny opdagelse kan muliggøre præcis forudsigelse af kræftspredning, før kræft udvikler sigVENSTRE:Spheroid af brystkræftceller, der bryder gennem basalmembranen for at invadere i det omkringliggende område. Denne evne bestemmes af forholdet mellem netrin-molekyler til stede i basalmembrans
Ny opdagelse kan muliggøre præcis forudsigelse af kræftspredning, før kræft udvikler sigVENSTRE:Spheroid af brystkræftceller, der bryder gennem basalmembranen for at invadere i det omkringliggende område. Denne evne bestemmes af forholdet mellem netrin-molekyler til stede i basalmembrans -
 En nemmere måde at spise grønt på:Vitamin B12 kan produceres under dejgæringKredit:CC0 Public Domain Vitamin B12 er et essentielt mikronæringsstof, der er nødvendigt for funktioner som vedligeholdelse af nervesystemet og dannelse af blodceller. Imidlertid, B12 findes hove
En nemmere måde at spise grønt på:Vitamin B12 kan produceres under dejgæringKredit:CC0 Public Domain Vitamin B12 er et essentielt mikronæringsstof, der er nødvendigt for funktioner som vedligeholdelse af nervesystemet og dannelse af blodceller. Imidlertid, B12 findes hove
- Skinflow:En blød robotskin baseret på væsketransmission
- Ny Jurassic ikke-fugle theropod dinosaur kaster lys over oprindelsen af flyvning i Dinosauria
- Al optisk kontrol af exciton -flow i et kolloidalt kvantebrøndskompleks
- Hvad er grøn tørrensning? En giftstofekspert forklarer
- Gastrointestinal-resident, formskiftende mikrodele til forlænget lægemiddeltilførsel
- Vikingernes metalhåndværk og ekspertise udviklede sig fra det 8. til det 9. århundrede


