Hvad er byggestenene i faste væsker og gasser?
Væsker: Væsker har et bestemt volumen, men de har ikke en bestemt form. De tager form af den beholder, de er i. Partiklerne i en væske er tæt sammen, men de er ikke så tæt pakket, som de er i et fast stof. Partiklerne i en væske kan bevæge sig forbi hinanden.
Gasser: Gasser har ikke en bestemt form eller volumen. De udvider sig for at fylde den beholder, de er i. Partiklerne i en gas er langt fra hinanden. Partiklerne i en gas kan nemt bevæge sig forbi hinanden.
Byggestenene i faste stoffer, væsker og gasser er atomer og molekyler. Atomer er de mindste enheder af stof, der stadig bevarer et grundstofs egenskaber. Molekyler er grupper af atomer, der holdes sammen af kemiske bindinger.
Et stofs stoftilstand afhænger af stoffets temperatur og tryk. Faste stoffer findes typisk ved lave temperaturer og høje tryk. Væsker findes typisk ved mellemliggende temperaturer og tryk. Gasser findes typisk ved høje temperaturer og lave tryk.
Der er nogle undtagelser fra disse regler. For eksempel kan vand eksistere som et fast stof, væske eller gas ved forskellige temperaturer og tryk.
Sidste artikelHvad er naturgas metan?
Næste artikelHvad er fællesnævneren i faste væsker og gasser?
 Varme artikler
Varme artikler
-
 En eksotisk mikrobe og en usædvanlig udvindingsproces kan tilføje op til en økonomisk måde at la…WPI kemiingeniørprofessor Michael Timko med en prøve af isobutanol. Han hjælper med at udvikle en ny proces, der kan tilbyde en mere økonomisk måde at lave dette lovende biobrændstof på, som kunne bru
En eksotisk mikrobe og en usædvanlig udvindingsproces kan tilføje op til en økonomisk måde at la…WPI kemiingeniørprofessor Michael Timko med en prøve af isobutanol. Han hjælper med at udvikle en ny proces, der kan tilbyde en mere økonomisk måde at lave dette lovende biobrændstof på, som kunne bru -
 Ny forskning giver mulighed for mere nøjagtig metamfetamindetektionKredit:Unsplash/CC0 Public Domain Metamfetamin er et stimulans, der kan tages som et rekreativt stof, enten ved injektioner eller rygning. Det er klassificeret som et klasse A-stof i Storbritannien
Ny forskning giver mulighed for mere nøjagtig metamfetamindetektionKredit:Unsplash/CC0 Public Domain Metamfetamin er et stimulans, der kan tages som et rekreativt stof, enten ved injektioner eller rygning. Det er klassificeret som et klasse A-stof i Storbritannien -
 Direkte metanomdannelse under milde forhold ved termo-, elektro- eller fotokatalyse gennemgåetMethans molekylære struktur (til venstre) og skematisk illustration af et energidiagram for lavtemperatur-metanaktivering i elektro- og fotoaktiveringsinvolverede reaktionssystemer (højre). Kredit:MEN
Direkte metanomdannelse under milde forhold ved termo-, elektro- eller fotokatalyse gennemgåetMethans molekylære struktur (til venstre) og skematisk illustration af et energidiagram for lavtemperatur-metanaktivering i elektro- og fotoaktiveringsinvolverede reaktionssystemer (højre). Kredit:MEN -
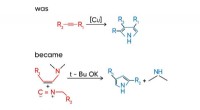 Kemikere foreslår en ny metode til syntese af pyrrolerEt team af kemikere fra RUDN University foreslog en ny metode til syntese af Pyrroles. Kredit:RUDN University En gruppe kemikere fra RUDN University foreslog en ny sikker tilgang til syntese af py
Kemikere foreslår en ny metode til syntese af pyrrolerEt team af kemikere fra RUDN University foreslog en ny metode til syntese af Pyrroles. Kredit:RUDN University En gruppe kemikere fra RUDN University foreslog en ny sikker tilgang til syntese af py
- Mens Facebook står over for ild, varmen dukker op på nr. 2 Sandberg
- Tidlig smeltning af vintersnefald fremmer det arktiske forår
- Virkningerne af kadmiumbelægning 304 rustfrit stål
- Hvor lang tid lever Crickets?
- Forskere udvikler et nanohybrid -køretøj til optimalt at levere medicin til menneskekroppen
- Gør enzymer egnede til industrielle anvendelser


