Hvilket volumen er optaget af 2,4 mol klor?
```
PV =nRT
```
hvor:
* P er trykket (i atmosfærer)
* V er volumen (i liter)
* n er antallet af mol
* R er den ideelle gaskonstant (0,08206 L * atm / mol * K)
* T er temperaturen (i Kelvin)
Ved at antage standard temperatur og tryk (STP), som er 0°C (273,15 K) og 1 atm, kan vi beregne volumen optaget af 2,4 mol klorgas:
```
V =nRT/P
=2,4 mol * 0,08206 L * atm / mol * K * 273,15 K / 1 atm
=55,12 L
```
Derfor fylder 2,4 mol klorgas et volumen på cirka 55,12 liter ved STP.
Sidste artikelEr svovldioxid en kovalent forbindelse?
Næste artikelHvilke produkter er lavet af polonium?
 Varme artikler
Varme artikler
-
 Stabile katalysatorer for ny energiCarina Brunnhofer (til venstre), Dominik Dworschak (til højre) Kredit:TU Wien På vej til en CO 2 -neutral økonomi, vi er nødt til at perfektionere en lang række teknologier – inklusive elektroke
Stabile katalysatorer for ny energiCarina Brunnhofer (til venstre), Dominik Dworschak (til højre) Kredit:TU Wien På vej til en CO 2 -neutral økonomi, vi er nødt til at perfektionere en lang række teknologier – inklusive elektroke -
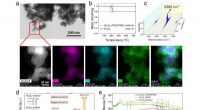 Direkte oxidativ overførselsproces bidrager til vandrensningProduktanalyser af modelreaktionssystemet (Co3 O4 /PMS/PhOH). et STEM, HAADF og EDS elementær kortlægningsbilleder af Co3 O4 efter reaktionen. b TGA-kurver for den uberørte og reagerede Co3 O4 i lufte
Direkte oxidativ overførselsproces bidrager til vandrensningProduktanalyser af modelreaktionssystemet (Co3 O4 /PMS/PhOH). et STEM, HAADF og EDS elementær kortlægningsbilleder af Co3 O4 efter reaktionen. b TGA-kurver for den uberørte og reagerede Co3 O4 i lufte -
 Symmetrisk spaltning af disulfider er hurtig og biokompatibelForskerholdet ledet af Frank Glorius bruger fotokatalysatorer og synligt lys til selektiv spaltning af svovl-svovlbindinger. Farven på reaktionsblandingen efter reaktionen kan give en første indikatio
Symmetrisk spaltning af disulfider er hurtig og biokompatibelForskerholdet ledet af Frank Glorius bruger fotokatalysatorer og synligt lys til selektiv spaltning af svovl-svovlbindinger. Farven på reaktionsblandingen efter reaktionen kan give en første indikatio -
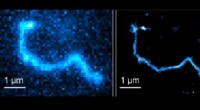 Nye træk for polymerkædedynamikSuperopløsnings fluorescensmikroskopi (højre) giver betydeligt skarpere billeder sammenlignet med konventionel fluorescensmikroskopi. Kredit:Abadi et al. En teknik, der gør det muligt for forskere
Nye træk for polymerkædedynamikSuperopløsnings fluorescensmikroskopi (højre) giver betydeligt skarpere billeder sammenlignet med konventionel fluorescensmikroskopi. Kredit:Abadi et al. En teknik, der gør det muligt for forskere
- Undersøgelse afdækker ny hindring for udvikling af immunterapier
- MIT kæmper med tidlige lederes holdning til indianere
- 1/3 af forældrene i 3 stater må ikke sende børn i skole på grund af COVID-19
- Sådan klæber du sensorer til huden uden klæbemiddel
- Små defekter i halvledere skabte fartbump for elektroner - forskere ryddede vejen
- Når en mængde elektricitet omdannes til at varme energien målt i hvad?


