Hvilken gruppe vil sandsynligvis reagere med klor i form af XCl?
Sidste artikelHvad er den balancerede ligning for fuldstændig forbrænding af ethanol i oxygen?
Næste artikelEr tinoxid et amfotert oxid?
 Varme artikler
Varme artikler
-
 Studiet giver mere end en million nye cykliske forbindelser, nogle med farmaceutisk potentialeUniversity of Illinois kemiprofessor Wilfred van der Donk og hans kolleger udviklede en ny metode til at generere store biblioteker af unikke cykliske forbindelser. Kredit:Don Hamerman Forskere si
Studiet giver mere end en million nye cykliske forbindelser, nogle med farmaceutisk potentialeUniversity of Illinois kemiprofessor Wilfred van der Donk og hans kolleger udviklede en ny metode til at generere store biblioteker af unikke cykliske forbindelser. Kredit:Don Hamerman Forskere si -
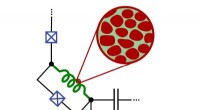 Granulært aluminium til fremtidige computereDen fluxonium-qubit, der indeholder granulært aluminium, kan forblive i en tilstand mellem 0 og 1 i en tid på op til 30 mikrosekunder (fig. Ioan Pop, SÆT) Computere baseret på kvantemekaniske prin
Granulært aluminium til fremtidige computereDen fluxonium-qubit, der indeholder granulært aluminium, kan forblive i en tilstand mellem 0 og 1 i en tid på op til 30 mikrosekunder (fig. Ioan Pop, SÆT) Computere baseret på kvantemekaniske prin -
 Brug af bakterier fra varme kilder, biokemiker studerer RNA-splejsning hos menneskerAaron Robart, Assisterende professor, WVU School of Medicine, Institut for Biokemi. Kredit:Aira Burkhart/West Virginia University Omkring 70 procent af det menneskelige genom koder ikke for noget.
Brug af bakterier fra varme kilder, biokemiker studerer RNA-splejsning hos menneskerAaron Robart, Assisterende professor, WVU School of Medicine, Institut for Biokemi. Kredit:Aira Burkhart/West Virginia University Omkring 70 procent af det menneskelige genom koder ikke for noget. -
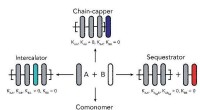 Styring af længden af supramolekylære polymererIllustration af, hvordan tilsætning af en anden supramolekylær polymer kan påvirke copolymerens længde. Kredit:Eindhoven University of Technology Systemer, der består af én supramolekylær polymer,
Styring af længden af supramolekylære polymererIllustration af, hvordan tilsætning af en anden supramolekylær polymer kan påvirke copolymerens længde. Kredit:Eindhoven University of Technology Systemer, der består af én supramolekylær polymer,
- Top 5 programmer, der finder nye anvendelser til gamle teknologier
- Google muliggør brug af Android -telefoner som en fysisk sikkerhedsnøgle
- Nikkel-78 bekræftede at være dobbelt magisk
- Elevernes trivsel begynder at falde fra det øjeblik, de går ind i gymnasiet
- Kunne diamanter være en computers bedste ven?
- Ældste australske menneske vendte tilbage til 42, 000 år gammel grav


