Vanddråber er opbygget af vandmolekyler, som er en forbindelse sammensat af to brintatomer og et oxygenatom (H2O). Hvert vandmolekyle består af to hydrogenatomer bundet til et oxygenatom. Iltatomet er lidt mere elektronegativt end hydrogenatomerne, hvilket betyder, at det tiltrækker elektroner stærkere. Dette skaber en asymmetrisk fordeling af ladning i molekylet, med en lille positiv ladning nær brintatomerne og en lille negativ ladning nær iltatomet. Dette får vandmolekyler til at være polære, hvilket betyder, at de har en positiv ende og en negativ ende. Den polære natur af vandmolekyler gør det muligt for dem at danne bindinger med hinanden gennem hydrogenbinding. Hydrogenbinding opstår, når den positive brintende af et vandmolekyle danner en binding med den negative iltende af et andet vandmolekyle. Disse hydrogenbindinger er ansvarlige for vands unikke egenskaber, såsom dets høje overfladespænding og høje specifikke varmekapacitet.
 Varme artikler
Varme artikler
 Skræddersyet kunstig perlemorEt tværsnit af en perlemor-imitation viser, at ved temperaturer på 800 grader Celsius og derover, der dannes knopper mellem blodpladerne, som størkner materialet. Kredit:Kunal Masania / ETH Zürich
Skræddersyet kunstig perlemorEt tværsnit af en perlemor-imitation viser, at ved temperaturer på 800 grader Celsius og derover, der dannes knopper mellem blodpladerne, som størkner materialet. Kredit:Kunal Masania / ETH Zürich Cellulært kraftværk genbruger affaldsgasserCODH/ACS-krystaller opnået uden oxygen. Den brune farve kommer fra de naturlige metaller, som proteinerne rummer. Kredit:Max Planck Institute for Marine Microbiology/T. Wagner Affaldsgasser fra ma
Cellulært kraftværk genbruger affaldsgasserCODH/ACS-krystaller opnået uden oxygen. Den brune farve kommer fra de naturlige metaller, som proteinerne rummer. Kredit:Max Planck Institute for Marine Microbiology/T. Wagner Affaldsgasser fra ma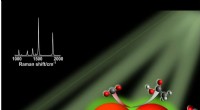 Lyshøstende nanopartikelkatalysatorer viser løfte i jagten på vedvarende kulstofbaserede brændst…Under de rette forhold, sølv nanopartikler, repræsenteret ved de store orange kugler, kan absorbere synligt lys. Ladningsbærere produceret ved lysexcitation overføres til CO2 og vand, tillader omdanne
Lyshøstende nanopartikelkatalysatorer viser løfte i jagten på vedvarende kulstofbaserede brændst…Under de rette forhold, sølv nanopartikler, repræsenteret ved de store orange kugler, kan absorbere synligt lys. Ladningsbærere produceret ved lysexcitation overføres til CO2 og vand, tillader omdanne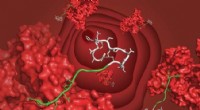 En ny ligand forlænger halveringstiden for peptider fra minutter til dageEt bicyklisk peptid (hvidt) bundet til serumalbumin (rødt) gennem den nyudviklede ligand (grøn), flyder i blodbanen. Kredit:C. Heinis/EPFL EPFL-forskere har udviklet et ligandmolekyle, der forbind
En ny ligand forlænger halveringstiden for peptider fra minutter til dageEt bicyklisk peptid (hvidt) bundet til serumalbumin (rødt) gennem den nyudviklede ligand (grøn), flyder i blodbanen. Kredit:C. Heinis/EPFL EPFL-forskere har udviklet et ligandmolekyle, der forbind

