Hvad er kogepunktet for natriumchloridopløsning?
Sidste artikelHvad bruges svovlpiller til?
Næste artikelHvor mange elektroner får svovl for at opnå ædelgaselektronkonfiguration?
 Varme artikler
Varme artikler
-
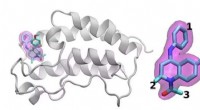 Forskningsgruppen bruger supercomputing til at målrette de mest lovende lægemiddelkandidater ud fr…En skematisk oversigt over BRD4 -proteinet bundet til et af 16 lægemidler baseret på det samme tetrahydroquinolin -stillads (fremhævet i magenta). Regioner, der er kemisk modificeret mellem de lægemid
Forskningsgruppen bruger supercomputing til at målrette de mest lovende lægemiddelkandidater ud fr…En skematisk oversigt over BRD4 -proteinet bundet til et af 16 lægemidler baseret på det samme tetrahydroquinolin -stillads (fremhævet i magenta). Regioner, der er kemisk modificeret mellem de lægemid -
 Bedre forståelse af principperne for siliciumætsning fører til forbedret overflademønsterVed hjælp af nøje udvalgte kombinationer af metaller, det er muligt at etse indviklede mønstre på en siliciumoverflade, som vist ovenfor. Kredit:Ref. 1 og licenseret under CC BY 4.0 © 2016 L. Kong et
Bedre forståelse af principperne for siliciumætsning fører til forbedret overflademønsterVed hjælp af nøje udvalgte kombinationer af metaller, det er muligt at etse indviklede mønstre på en siliciumoverflade, som vist ovenfor. Kredit:Ref. 1 og licenseret under CC BY 4.0 © 2016 L. Kong et -
 Langrødt fluorescerende silke kan dræbe skadelige bakterier som biomedicinsk og miljømæssigt mid…Når et grønt lys skinner på rød fluorescerende silke, en mekanisme til at dræbe patogener aktiveres. Kredit:Purdue University image/Jung Woo Leem Et silkehybridmateriale angriber bakterier, når de
Langrødt fluorescerende silke kan dræbe skadelige bakterier som biomedicinsk og miljømæssigt mid…Når et grønt lys skinner på rød fluorescerende silke, en mekanisme til at dræbe patogener aktiveres. Kredit:Purdue University image/Jung Woo Leem Et silkehybridmateriale angriber bakterier, når de -
 Opsugning af lægemidler og produkter til personlig pleje fra vandKredit:American Chemical Society Medicin, der udskilles i urinen eller dumpes i toilettet, kan ende i vandforsyningen, ligesom lotioner eller kosmetik, der vasker kroppen af og går ned i vasken
Opsugning af lægemidler og produkter til personlig pleje fra vandKredit:American Chemical Society Medicin, der udskilles i urinen eller dumpes i toilettet, kan ende i vandforsyningen, ligesom lotioner eller kosmetik, der vasker kroppen af og går ned i vasken
- Undersøgelse af de mange smagsvarianter af spiselige myrer
- At ignorere klimaændringer er lige blevet dyrere
- Forskere:Kulturel afbrænding er bedre for australsk jord end foreskrevet afbrænding, eller slet in…
- Står ugifte kvinder over for mangel på partnere på det amerikanske ægteskabsmarked?
- Perfektionistiske elever får højere karakterer, men til hvilken pris?
- Hvordan kan du måle og beskrive nedbørsskydække på en given dag?


