Hvad er en ionisk forbindelse so2 clo2 h2o2 tio2?
Af de fire forbindelser, du har angivet, er det kun TiO$_2$ er en ionisk forbindelse. Den består af positivt ladede titaniumioner (Ti$^{4+}$) og negativt ladede oxidioner (O$^{2-}$). Den stærke elektrostatiske tiltrækning mellem titanium- og oxidionerne danner den stabile ionforbindelse TiO$_2$.
På den anden side er SO$_2$, ClO$_2$ og H$_2$O$_2$ molekylære forbindelser , ikke ioniske forbindelser. I disse forbindelser er atomer kovalent bundet og deler elektroner for at opnå en stabil elektronkonfiguration. Der er ingen overførsel af elektroner eller dannelse af ioner i disse tilfælde.
Her er en oversigt over forbindelserne:
- TiO$_2$ :Ionisk forbindelse (titaniumdioxid)
- SO$_2$ :Molekylær forbindelse (svovldioxid)
- ClO$_2$ :Molekylær forbindelse (chlordioxid)
- H$_2$O$_2$ :Molekylær forbindelse (brintoverilte)
 Varme artikler
Varme artikler
-
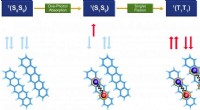 Banebrydende kvantekemiteknik til beregningsdesign og optimering af organiske fotofunktionelle mater…Billede 1. Singlet-fissionsprocessen i pentacen-dimer:den indledende singlet-exciton S1S0 af en monomer deler sig i to frie triplet-excitoner T1-T1 via et korreleret triplet-par 1 (TT) ligeligt fordel
Banebrydende kvantekemiteknik til beregningsdesign og optimering af organiske fotofunktionelle mater…Billede 1. Singlet-fissionsprocessen i pentacen-dimer:den indledende singlet-exciton S1S0 af en monomer deler sig i to frie triplet-excitoner T1-T1 via et korreleret triplet-par 1 (TT) ligeligt fordel -
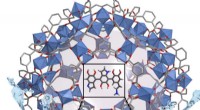 Fjernelse af tungmetaller fra vand med MOF'erEn organisk metalramme kan fjerne bly fra vandprøver, få dem til EPA-godkendte niveauer på få sekunder. Kredit:American Chemical Society Det anslås, at 1 milliard mennesker ikke har adgang til ren
Fjernelse af tungmetaller fra vand med MOF'erEn organisk metalramme kan fjerne bly fra vandprøver, få dem til EPA-godkendte niveauer på få sekunder. Kredit:American Chemical Society Det anslås, at 1 milliard mennesker ikke har adgang til ren -
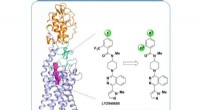 Forskere dechifrerer multi-domænet, struktur i fuld længde af den menneskelige glattede receptorStruktur af multi-domæne human Smoothened receptor, et vigtigt lægemiddelmål for kræftsygdomme. Kredit:ShanghaiTech University Et team af forskere ledet af iHuman Institute of ShanghaiTech Univers
Forskere dechifrerer multi-domænet, struktur i fuld længde af den menneskelige glattede receptorStruktur af multi-domæne human Smoothened receptor, et vigtigt lægemiddelmål for kræftsygdomme. Kredit:ShanghaiTech University Et team af forskere ledet af iHuman Institute of ShanghaiTech Univers -
 Undersøgelse finder beviser for eksistensen af undvigende metabolonKredit:CC0 Public Domain I mere end 40 år, videnskabsmænd har antaget eksistensen af enzymklynger, eller metaboloner, ved at lette forskellige processer i celler. Ved hjælp af en ny billedtekno
Undersøgelse finder beviser for eksistensen af undvigende metabolonKredit:CC0 Public Domain I mere end 40 år, videnskabsmænd har antaget eksistensen af enzymklynger, eller metaboloner, ved at lette forskellige processer i celler. Ved hjælp af en ny billedtekno
- Fra losseplads til læbestift:Vindrueaffald som kosmetik og fødevareingrediens
- Hvad er funktionen ved at spore farvestof ved gelelektroforese?
- Termiske egenskaber af pap
- Underlig elektronadfærd bliver endnu mere underlig:Ladningsfraktionalisering observeret spektroskop…
- Mediestereotyper forvirrer børns videnskabelige ambitioner
- Sådan tilføjes fragmenter, der har forskellige betegnelser


