Et bariumatom opnår en stabil elektronkonfiguration, når det binder sig til?
Sidste artikelEr rent kalium metallisk eller kovalent?
Næste artikelForklar Hvordan danner atomet af magnesium og klor ioner?
 Varme artikler
Varme artikler
-
 Materialeforskere viser måde at lave holdbare kunstige sener fra forbedrede hydrogelerMikroskopisk foto af det kunstige senemateriale udviklet af UCLA-materialeforskere. Forbedret til at bringe detaljer frem. Ægte skala af billedet er 1 cm i bredden. Kredit:Sidi Duan, Shuwang Wu, Mutia
Materialeforskere viser måde at lave holdbare kunstige sener fra forbedrede hydrogelerMikroskopisk foto af det kunstige senemateriale udviklet af UCLA-materialeforskere. Forbedret til at bringe detaljer frem. Ægte skala af billedet er 1 cm i bredden. Kredit:Sidi Duan, Shuwang Wu, Mutia -
 Forskere udvikler et værktøj til at undersøge plastadfærd ned til molekylær skalaPrinceton-forskere, herunder ph.d.-studerende Dane Christie, som nu er materialeforsker i Corning, har udviklet et værktøj til at undersøge polymerer på molekylær skala. Kredit:Corning Inc Overvej
Forskere udvikler et værktøj til at undersøge plastadfærd ned til molekylær skalaPrinceton-forskere, herunder ph.d.-studerende Dane Christie, som nu er materialeforsker i Corning, har udviklet et værktøj til at undersøge polymerer på molekylær skala. Kredit:Corning Inc Overvej -
 De udvidede muligheder for biobaserede polymererKredit:Institut for Kemisk Forskning i Catalonien At finde innovative og bæredygtige løsninger til vores materialebehov er et af kernemålene for grøn kemi. De utallige plastik, der omslutter vores
De udvidede muligheder for biobaserede polymererKredit:Institut for Kemisk Forskning i Catalonien At finde innovative og bæredygtige løsninger til vores materialebehov er et af kernemålene for grøn kemi. De utallige plastik, der omslutter vores -
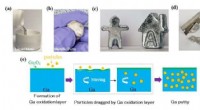 Spartellignende kompositter af galliummetal med potentiale til anvendelse i virkeligheden(a) Flydende gallium hældes i en beholder. (b) Galliumkitt støbes til en kugle. (c) Forskellige figurer fremstillet af galliumspartel. (d) Galliumspartel skæres af et blad. (e) Mekanismen for dannelse
Spartellignende kompositter af galliummetal med potentiale til anvendelse i virkeligheden(a) Flydende gallium hældes i en beholder. (b) Galliumkitt støbes til en kugle. (c) Forskellige figurer fremstillet af galliumspartel. (d) Galliumspartel skæres af et blad. (e) Mekanismen for dannelse
- Forskere ved Brasiliens ruminstitut opdager, hvorfor lynet forgrener sig og flimrer
- Ny forskning viser, at førskoleundervisning af høj kvalitet reducerer behovet for senere specialud…
- Astronomer opdager en klasse af mærkelige objekter nær vores galaksers enorme sorte hul
- Nordamerikansk iskappeforfald mindskede klimavariabiliteten på den sydlige halvkugle
- Musikalsk sensor viser, at dårlig medicin spiller falsk tone
- Snapchat opgraderer briller efter første generations flop


