Hvad er et opløsningsmiddel i eksperimentet?
Her er en sammenbrud:
* opløst: Det stof, der bliver opløst. Det kan være en solid, flydende eller gas.
* opløsningsmiddel: Det stof, der opløses. Det er normalt en væske, men kan også være en gas eller et fast stof.
* Løsning: Den homogene blanding dannet, når opløsningen opløses i opløsningsmidlet.
Eksempler:
* vand er et almindeligt opløsningsmiddel for mange stoffer, som sukker (opløst) for at fremstille en sukkeropløsning.
* acetone er et opløsningsmiddel, der bruges til at opløse neglelak.
* ethanol er et opløsningsmiddel, der bruges til at udtrække æteriske olier fra planter.
Vigtige punkter om opløsningsmidler i eksperimenter:
* opløselighed: Et opløst stof til at opløses i et opløsningsmiddel kaldes opløselighed. Forskellige opløste stoffer har forskellige opløseligheder i forskellige opløsningsmidler.
* Polaritet: Opløsningsmidler kan være polære eller ikke-polære. Polære opløsningsmidler (som vand) opløser polære opløste stoffer (som sukker), mens ikke-polære opløsningsmidler (som olie) opløser ikke-polære opløste stoffer (som fedt).
* Koncentration: Mængden af opløst stof, der er opløst i en given mængde opløsningsmiddel, bestemmer koncentrationen af opløsningen.
I et eksperiment er opløsningsmidlet vigtigt, fordi det:
* giver et medium til at der kan forekomme reaktioner.
* hjælper med at kontrollere reaktionshastigheden.
* muliggør adskillelse og oprensning af stoffer.
* kan bruges til at udtrække ønskede forbindelser fra en blanding.
At forstå opløsningsmidlernes rolle i eksperimenter er afgørende for at designe vellykkede eksperimenter og fortolke resultaterne nøjagtigt.
 Varme artikler
Varme artikler
-
 Tyndt lag beskytter batteriet, tillader kold opladningLagene i en lithiummetalanode til lavtemperaturbatterier Kredit:Donghai Wang, Penn State I jagten på en pålidelig, hurtig opladning, koldt vejr batteri til biler, en selvsamlende, et tyndt lag af
Tyndt lag beskytter batteriet, tillader kold opladningLagene i en lithiummetalanode til lavtemperaturbatterier Kredit:Donghai Wang, Penn State I jagten på en pålidelig, hurtig opladning, koldt vejr batteri til biler, en selvsamlende, et tyndt lag af -
 Forskere skaber en mere effektiv hydrogel til at hele sårElektronmikroskopbillede af den porøse hydrogel. Kredit:UNH Forskere ved University of New Hampshire har skabt en nem at lave, lavpris injicerbar hydrogel, der kan hjælpe sår med at hele hurtigere
Forskere skaber en mere effektiv hydrogel til at hele sårElektronmikroskopbillede af den porøse hydrogel. Kredit:UNH Forskere ved University of New Hampshire har skabt en nem at lave, lavpris injicerbar hydrogel, der kan hjælpe sår med at hele hurtigere -
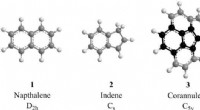 Interstellar kemi:lavtemperaturgasfasedannelse af inden i det interstellare mediumDe enkleste repræsentanter for to-ring PAHer, der bærer to seks-leddede (naphthalen, C10H8; 1) og en seks- sammen med en fem-leddet ring (indene, C9H8; 2). Mens hydrogenabstraktion-vinylacetylen-addit
Interstellar kemi:lavtemperaturgasfasedannelse af inden i det interstellare mediumDe enkleste repræsentanter for to-ring PAHer, der bærer to seks-leddede (naphthalen, C10H8; 1) og en seks- sammen med en fem-leddet ring (indene, C9H8; 2). Mens hydrogenabstraktion-vinylacetylen-addit -
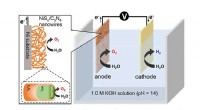 Et skridt nærmere en brintdrevet økonomi ved hjælp af en effektiv anode til vandopdelingSkematisk repræsentation af vanddissociationsprocessen ved lavt overpotentiale på ca. 32 mV ved anvendelse af NiS x nanotråde proppet ind i C 3 N 4 skede som anode til vandoxidation. Kredit:Niig
Et skridt nærmere en brintdrevet økonomi ved hjælp af en effektiv anode til vandopdelingSkematisk repræsentation af vanddissociationsprocessen ved lavt overpotentiale på ca. 32 mV ved anvendelse af NiS x nanotråde proppet ind i C 3 N 4 skede som anode til vandoxidation. Kredit:Niig
- Forskere ændrer membranproteiner for at gøre dem nemmere at studere
- Virtuel lufthavn for at forbedre tilgængeligheden for passagerer med yderligere mobilitetsbehov
- Hvordan Burger King afslørede stemmeassistenternes hackbarhed
- Tropisk storm, flod oversvømmelser hammer Golf miljø
- Flyvende blind:Apps hjælper synshandicappede med at navigere i lufthavnen
- En skelsættende undersøgelse viser, hvordan børnetilskud styrker kvinder i Brasilien og Sydafrika


