Hvordan vises loven om bevaringsmasse af en afbalanceret kemisk reaktion?
* Repræsenterer de kemiske formler: De kemiske formler i en afbalanceret ligning repræsenterer nøjagtigt atomer og molekyler involveret i reaktionen.
* opretholdelse af lige antal af hver type atom: Koefficienterne foran hver kemisk formel sikrer, at det samme antal atomer i hvert element er til stede på begge sider af ligningen.
her er et simpelt eksempel:
Forbrændingen af methan (CH4) med ilt (O2) producerer kuldioxid (CO2) og vand (H2O).
Ubalanceret ligning:
CH4 + O2 → CO2 + H2O
afbalanceret ligning:
CH4 + 2O2 → CO2 + 2H2O
Forklaring:
* reaktanter: På venstre side har vi et carbonatom (C), fire hydrogenatomer (H) og to iltatomer (O).
* Produkter: På højre side har vi også et carbonatom (C), fire hydrogenatomer (H) og fire iltatomer (O).
Ved at afbalancere ligningen sikrer vi, at det samme antal af hver atomtype findes på begge sider. Dette betyder, at den samlede masse af reaktanterne (metan og ilt) skal svare til den samlede masse af produkterne (kuldioxid og vand). Ingen atomer går tabt eller opnås under reaktionen, kun omarrangeret, hvilket bekræfter loven om bevarelse af masse.
 Varme artikler
Varme artikler
-
 Jane Austen -citat kodet i en polymerEt citat fra Jane Austens Mansfield Park skrevet i oligourethanes. Kredit:Sarah Moor Ved hjælp af en ny molekylær datalagringsteknik, forskere ved University of Texas i Austin har kodet et citat f
Jane Austen -citat kodet i en polymerEt citat fra Jane Austens Mansfield Park skrevet i oligourethanes. Kredit:Sarah Moor Ved hjælp af en ny molekylær datalagringsteknik, forskere ved University of Texas i Austin har kodet et citat f -
 Slette lidt kemi fra historienEn ny undersøgelse foretaget af et forskerhold ved University of Western Australia og Murdoch University har fundet ud af, at en ion, der betragtes som en væsentlig del af kemiberegninger, ikke eksist
Slette lidt kemi fra historienEn ny undersøgelse foretaget af et forskerhold ved University of Western Australia og Murdoch University har fundet ud af, at en ion, der betragtes som en væsentlig del af kemiberegninger, ikke eksist -
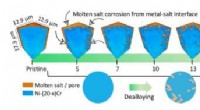 Forskere ser smeltede salte skære små kroge og tunneler ind i metallegeringer i 3DIllustrationen viser, hvordan smeltet salt over tid fjerner metallisk materiale (blå) fra prøven i 3D (øvre) og 2D -visualiseringer (nedre). Denne proces, såkaldt dealloying skaber et bikontinuerligt
Forskere ser smeltede salte skære små kroge og tunneler ind i metallegeringer i 3DIllustrationen viser, hvordan smeltet salt over tid fjerner metallisk materiale (blå) fra prøven i 3D (øvre) og 2D -visualiseringer (nedre). Denne proces, såkaldt dealloying skaber et bikontinuerligt -
 Det nye garn?!—Bærbart, vaskbare tekstilenheder er mulige med MXene-coated garnForskere fra Drexel Universitys College of Engineering og Center for Functional Fabrics har udviklet en måde at belægge garn med ledende MXene-materialer for at lave holdbare funktionelle tekstiler. K
Det nye garn?!—Bærbart, vaskbare tekstilenheder er mulige med MXene-coated garnForskere fra Drexel Universitys College of Engineering og Center for Functional Fabrics har udviklet en måde at belægge garn med ledende MXene-materialer for at lave holdbare funktionelle tekstiler. K
- Hvad er antallet af calciumatomer i chlorid?
- Fremtiden ser lys ud for kulstof nanorør-solceller
- Satellitter hjælper med at kigge ind i orkaner
- Mysteriet om usædvanligt neutronstjernesystem afsløret efter 20 år, tak til tusindvis af frivilli…
- Global opvarmning fundet at være skyld i risikoen for oversvømmelser i de peruvianske Andesbjerge,…
- De fleste amerikanere har ikke nok aktiver til at modstå 3 måneder uden indkomst


