Hvordan forklarer du det særegne ved saltholdighed af havvand og på lignende måde for hårdhedsvand?
saltholdighed af havvand:
særegenhed: Havvand er salt med en gennemsnitlig saltholdighed på omkring 3,5%. Dette betyder, at 35 gram for hver 1000 gram havvand opløses.
Forklaring:
* forvitring og erosion: Klipper på land er konstant forvitret og eroderet af regn, vind og floder. Disse processer frigiver opløste mineraler og salte, der føres i havet.
* Hydrotermiske ventilationsåbninger: Undervandsvulkaner og hydrotermiske åbninger frigiver opløste mineraler og salte i havet.
* Vulkanudbrud: Vulkanudbrud kan også frigive betydelige mængder salte i atmosfæren, som til sidst falder i havet som regn.
* Fordampning og nedbør: Når havvand fordamper, forbliver de opløste salte bagud, hvilket øger saltholdigheden af det resterende vand. Imidlertid er denne proces afbalanceret ved nedbør, der fortynder saltkoncentrationen.
* balance mellem input og output: Saltholdigheden af havvand opretholdes af en balance mellem indgange af salte og output, såsom dannelse af havsaltaflejringer og fjernelse af salte af organismer.
Faktorer, der påvirker saltholdigheden:
* breddegrad: Saltholdigheden er generelt højere i varmere, tørrere regioner på grund af øget fordampning.
* placering: Saltholdigheden varierer afhængigt af placeringen, påvirket af faktorer som flodstrøm, nærhed til issmeltning og havstrømme.
* dybde: Saltholdigheden kan variere med dybde, hvor overfladelaget typisk er mindre saltvand end dybere lag.
Hårdhed af vand:
særegenhed: Hårdt vand indeholder høje koncentrationer af opløste mineraler, primært calcium og magnesium.
Forklaring:
* Geologisk dannelse: Vandets rejse gennem jorden, især gennem kalksten- og dolomitformationer, opløser disse mineraler.
* forvitring og opløsning: Regnvand er let surt, så det kan opløse calcium og magnesium fra klipper.
* menneskelige aktiviteter: Industrielle processer, såsom minedrift og landbrug, kan bidrage til hårdheden af vand ved at frigive mineraler i vandforsyningen.
Typer af hårdhed:
* Midlertidig hårdhed: Forårsaget af opløst calcium- og magnesiumbicarbonater. Det kan fjernes ved at koge vandet.
* Permanent hårdhed: Forårsaget af opløst calcium- og magnesiumsulfater og chlorider. Kogning fjerner det ikke.
Konsekvenser af hårdt vand:
* skala dannelse: Hårdt vand kan danne skalaaflejringer i rør og apparater, reducere effektiviteten og potentielt forårsage skade.
* sæbe skum: Hårdt vand reagerer med sæbe for at danne en hvid, sæbestrester.
* tør hud og hår: Hårdt vand kan fjerne naturlige olier fra hud og hår, hvilket får dem til at føle sig tørre og sprøde.
Både saltholdighed og vandhårdhed er vigtige faktorer, der skal overvejes i forskellige sammenhænge, fra menneskers sundhed og landbrug til industrielle processer og miljømæssig bæredygtighed. At forstå de særegenheder og oprindelsen af disse egenskaber hjælper os med at styre vandressourcer effektivt og adressere relaterede udfordringer.
Sidste artikelHvilket stof er partiklerne længst fra hinanden?
Næste artikelHvad produceres på Rivosomes?
 Varme artikler
Varme artikler
-
 En detektivhistorie om skovbrande og vinKredit:CC0 Public Domain I denne historie om vin- og røglugt, alle kender whodunit - det er røgen fra skovbrande. Men det er hvordan, der har fået forskere og vinmagere til at stoppe. Ifølge en ar
En detektivhistorie om skovbrande og vinKredit:CC0 Public Domain I denne historie om vin- og røglugt, alle kender whodunit - det er røgen fra skovbrande. Men det er hvordan, der har fået forskere og vinmagere til at stoppe. Ifølge en ar -
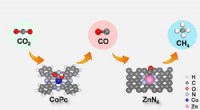 Tandemkatalysator til forbedring af kuldioxidelektroreduktion til metanCO2 reduceres først elektrokemisk til CO og derefter diffunderer CO til Zn-N-C for yderligere omdannelse til CH 4 over CoPc@Zn-N-C tandemkatalysator. Kredit:LIN Long og LIU Tianfu Kuldioxidreduk
Tandemkatalysator til forbedring af kuldioxidelektroreduktion til metanCO2 reduceres først elektrokemisk til CO og derefter diffunderer CO til Zn-N-C for yderligere omdannelse til CH 4 over CoPc@Zn-N-C tandemkatalysator. Kredit:LIN Long og LIU Tianfu Kuldioxidreduk -
 Kunstig intelligens identificerer den optimale materialeformelEt kig ind i sprutsystemet, hvor nanostrukturerede lag genereres. Kredit:Lars Banko Nanostrukturerede lag kan prale af utallige potentielle egenskaber - men hvordan kan den bedst egnede identifice
Kunstig intelligens identificerer den optimale materialeformelEt kig ind i sprutsystemet, hvor nanostrukturerede lag genereres. Kredit:Lars Banko Nanostrukturerede lag kan prale af utallige potentielle egenskaber - men hvordan kan den bedst egnede identifice -
 3-D katalysatorer til forbedrede hydrazinfrie drivmidlerKredit:RHEFORM Hydrazin, et af de mest udbredte flydende drivmidler til rumfremdrivningssystemer, er også ekstremt giftig. EU-forskere har udviklet 3D-katalysatorer til antændelse af alternative d
3-D katalysatorer til forbedrede hydrazinfrie drivmidlerKredit:RHEFORM Hydrazin, et af de mest udbredte flydende drivmidler til rumfremdrivningssystemer, er også ekstremt giftig. EU-forskere har udviklet 3D-katalysatorer til antændelse af alternative d
- Forskere anvender kemiske værktøjer til at opdage kræftfremkaldende proteiner
- NASA udforsker potentialet for ændrede virkeligheder for rumteknik og videnskab
- Temperatur, fugtighed, vind forudsiger anden pandemibølge
- Ny forskning undersøger, hvordan curling er landdistrikternes klippe
- Forældre får lynkursus i fjernundervisningsdilemmaer
- Hvad er MER? Det er en måde at måle kvantematerialer på, og det fortæller os nye og interessante…


