Hvilket stof er partiklerne længst fra hinanden?
Her er hvorfor:
* Gasser: Gaspartikler har meget svage attraktive kræfter mellem dem. De bevæger sig frit og tilfældigt og kolliderer med hinanden og væggene i deres beholder. Dette resulterer i meget plads mellem partiklerne.
* væsker: Væsker har stærkere attraktive kræfter end gasser. Partiklerne er tættere sammen og kan bevæge sig rundt om hinanden, men de er ikke så frie som gaspartikler.
* faste stoffer: Faststoffer har de stærkeste attraktive kræfter. Partiklerne er tæt pakket og vibrerer i faste positioner.
Så i resuméet, jo længere fra hinanden er partiklerne, jo svagere de attraktive kræfter mellem dem, og jo mere sandsynligt er stoffet at være i en gasformig tilstand.
 Varme artikler
Varme artikler
-
 Naturen er en nøgle til at afvise væskerBefugtende overflader med mikrosøjler (til venstre) mister deres omnifobicitet, når de beskadiges, mens mikroteksturer med dobbelt tilbagevendende hulrum (højre) udviser omnifobicitet trods lokalisere
Naturen er en nøgle til at afvise væskerBefugtende overflader med mikrosøjler (til venstre) mister deres omnifobicitet, når de beskadiges, mens mikroteksturer med dobbelt tilbagevendende hulrum (højre) udviser omnifobicitet trods lokalisere -
 Kemikere foreslår ny gavnlig katalysator til indledende materialer i apoteketCyanosilylering af aldehyder. Kredit:Atash Gurbanov Et samarbejde mellem forskere fra RUDN University (Rusland), Centro de Química Estrutura (Portugal) og Baku State University (Aserbajdsjan) fore
Kemikere foreslår ny gavnlig katalysator til indledende materialer i apoteketCyanosilylering af aldehyder. Kredit:Atash Gurbanov Et samarbejde mellem forskere fra RUDN University (Rusland), Centro de Química Estrutura (Portugal) og Baku State University (Aserbajdsjan) fore -
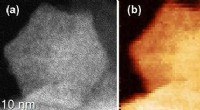 Mangan kan endelig løse problem med brintbrændstofcellerBilledet til venstre viser mangankatalysatorpartikelform. De rigtige billeder viser den ensartede elementære fordeling af kulstof gennem partiklen. Kredit:Gang Wu, Universitetet i Buffalo. Mangan
Mangan kan endelig løse problem med brintbrændstofcellerBilledet til venstre viser mangankatalysatorpartikelform. De rigtige billeder viser den ensartede elementære fordeling af kulstof gennem partiklen. Kredit:Gang Wu, Universitetet i Buffalo. Mangan -
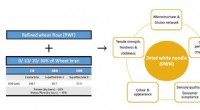 Nudler beriget med kostfibre af avanceret teknologi forbliver velsmagendeFigur 1:Grafisk repræsentation af de (venstre) eksperimentelle parametre og de (højre) attributter studeret som en del af denne forskning. Kredit:National University of Singapore NUS-fødevareforsk
Nudler beriget med kostfibre af avanceret teknologi forbliver velsmagendeFigur 1:Grafisk repræsentation af de (venstre) eksperimentelle parametre og de (højre) attributter studeret som en del af denne forskning. Kredit:National University of Singapore NUS-fødevareforsk
- Reagerer brint med saltsyre?
- Når kopierer kromosomer i løbet af en livscyklus?
- Rekordlav 2016 havis i Antarktis på grund af perfekt tropisk storm, polære forhold
- Hvad er tre specifikke grunde til, at videnskab er vigtig?
- Vores energisult er knyttet til vores økonomiske fortid:undersøgelse
- Hvad er gitterkoordinaterne for Little Rock Arkansas?


