Er et atom med seks elektroner mere stabile end én?
* stabilitet er relativ: Atomer stræber efter en stabil elektronkonfiguration, normalt ved at have en fuld ydre skal af elektroner.
* Antal elektroner er ikke den eneste faktor: Antallet af protoner (som bestemmer elementet) og arrangementet af elektroner (i orbitaler) er afgørende for stabilitet.
Eksempler:
* carbon (6 protoner): Carbon har 6 elektroner. Det er ikke særlig stabilt på egen hånd, da den kun har 4 i sin ydre skal. Det har en tendens til at danne bindinger med andre atomer for at opnå en fuld ydre skal.
* nitrogen (7 protoner): Nitrogen har 7 elektroner. Det er mere stabilt end kulstof, fordi dets ydre skal har 5 elektroner, hvilket betyder, at det kun er en væk fra en fuld skal.
* neon (10 protoner): Neon har 10 elektroner med en fuld ydre skal. Det er meget stabilt og eksisterer som en ædel gas.
Konklusion:
Et atom med seks elektroner kan være * mere stabilt * end et atom med et elektron, men det er ikke en garanti. Stabilitet afhænger af elementet og dets elektronkonfiguration.
Sidste artikelEr den ydre skal af nikkel fuld?
Næste artikelHvad har forudsigelige kemiske egenskaber?
 Varme artikler
Varme artikler
-
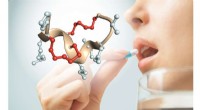 Peptider, der kan tages som en pilleStruktur af et dobbeltbro-peptid, der ikke nedbrydes af enzymer i mave og tarme. De to stabiliserende kemikaliebroer er vist med rødt. Kredit:C. Heinis (EPFL) Peptider er korte kæder af aminosyrer
Peptider, der kan tages som en pilleStruktur af et dobbeltbro-peptid, der ikke nedbrydes af enzymer i mave og tarme. De to stabiliserende kemikaliebroer er vist med rødt. Kredit:C. Heinis (EPFL) Peptider er korte kæder af aminosyrer -
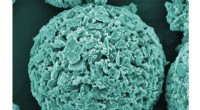 Nye materialer og processer til at rense patogene mikroorganismer fra vandEmpa -forskere udvikler nye filtersystemer fremstillet af kompositmaterialer såsom keramiske granulater med en kobber -nanokoating som afbildet her (elektronmikroskopi, farvet). Kredit:Sena Yüzbasi /
Nye materialer og processer til at rense patogene mikroorganismer fra vandEmpa -forskere udvikler nye filtersystemer fremstillet af kompositmaterialer såsom keramiske granulater med en kobber -nanokoating som afbildet her (elektronmikroskopi, farvet). Kredit:Sena Yüzbasi / -
 En havændring for plastikforurening:nyt materiale nedbrydes biologisk i havvandEn bæredygtig Blueview-sko nedbrydes biologisk i havvand efter 11 uger. Kredit:Daniel Zhen, Algenesis Inc. Plast, der nu er allestedsnærværende i den moderne verden, er blevet en stigende trussel m
En havændring for plastikforurening:nyt materiale nedbrydes biologisk i havvandEn bæredygtig Blueview-sko nedbrydes biologisk i havvand efter 11 uger. Kredit:Daniel Zhen, Algenesis Inc. Plast, der nu er allestedsnærværende i den moderne verden, er blevet en stigende trussel m -
 Ny metode hjælper med at kvantificere reversibilitet og irreversibilitet af praktiske Li-metalbatte…Metoden til afkobling og kvantificering af aktiv Li og død Li. Kredit:NIMTE En forskergruppe ledet af prof. Liu Zhaoping ved Ningbo Institute of Materials Technology and Engineering (NIMTE) under d
Ny metode hjælper med at kvantificere reversibilitet og irreversibilitet af praktiske Li-metalbatte…Metoden til afkobling og kvantificering af aktiv Li og død Li. Kredit:NIMTE En forskergruppe ledet af prof. Liu Zhaoping ved Ningbo Institute of Materials Technology and Engineering (NIMTE) under d
- Wide learning AI-teknologi muliggør meget præcis læring selv fra ubalancerede datasæt
- Sådan beregnes friktionsmoment
- Hvorfor får laboratoriebordplader en syrefast belægning?
- Ny open access database for middelalderlitteratur
- Hvad er tændt eller slukket af regulatoriske proteiner?
- Undersøgelse konstaterer, at restaurering af Nachusa-græsland fungerer i jorden, også


