Er den ydre skal af nikkel fuld?
Her er hvorfor:
* Nickels elektronkonfiguration: Nikkel har et atomnummer på 28, hvilket betyder, at det har 28 elektroner. Dens elektronkonfiguration er [AR] 3D⁸ 4S².
* taber elektroner til dannelse af en ion: For at opnå en stabil konfiguration mister nikkel sine to 4S -elektroner og bliver Ni²⁺.
* fuld ydre skal: Dette efterlader nikkel med elektronkonfigurationen [AR] 3D⁸, der ligner den stabile konfiguration af argon. 3D -skallen kan holde op til 10 elektroner, og nu har nikkel en fuld ydre skal.
Vigtig note: Dette gælder for den * ioniske * form for nikkel. I sin * neutrale * tilstand er Nickels ydre skal ikke Fuld, da det har to elektroner i 4S -skallen.
Sidste artikelHvor mange flere valenselektroner skal ilt have en fuld ydre?
Næste artikelEr et atom med seks elektroner mere stabile end én?
 Varme artikler
Varme artikler
-
 Simpel teknik giver stærkere polymererForskere har fundet en ny tilgang til at reducere antallet af sløjfer (røde) i en polymer. Metoden kunne tilbyde en nem måde for producenter af industrielt anvendelige materialer som plast eller geler
Simpel teknik giver stærkere polymererForskere har fundet en ny tilgang til at reducere antallet af sløjfer (røde) i en polymer. Metoden kunne tilbyde en nem måde for producenter af industrielt anvendelige materialer som plast eller geler -
 Dalian kohærent lyskilde afslører iltproduktion fra tre-legeme fotodissociation af vandDalian Coherent Light Source afslører tre-legeme fotodissociation af vand som en vigtig præbiotisk-O2 kilde. Kredit:DICP Herkomsten af ilt på Jorden og andre solar planetariske legemer er et gru
Dalian kohærent lyskilde afslører iltproduktion fra tre-legeme fotodissociation af vandDalian Coherent Light Source afslører tre-legeme fotodissociation af vand som en vigtig præbiotisk-O2 kilde. Kredit:DICP Herkomsten af ilt på Jorden og andre solar planetariske legemer er et gru -
 Biokemisk superlim åbner en ny tilgang til vaccineudviklingKredit:University of Oxford Et spinoutfirma fra Oxford University er ved at udvikle en molekylær superlim til hurtig udvikling af vacciner rettet mod en række sygdomme. SpyBiotech bruger biokemis
Biokemisk superlim åbner en ny tilgang til vaccineudviklingKredit:University of Oxford Et spinoutfirma fra Oxford University er ved at udvikle en molekylær superlim til hurtig udvikling af vacciner rettet mod en række sygdomme. SpyBiotech bruger biokemis -
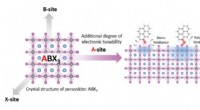 Ny måde at tænde for nanomaterialer til elektroniske applikationerSkematisk af perovskit materiale med organiske molekyler, der kan tilføje til dets elektroniske egenskaber. Kredit:Jingjing Xue og Rui Wang/UCLA Samueli School of Engineering UCLA materialeforsker
Ny måde at tænde for nanomaterialer til elektroniske applikationerSkematisk af perovskit materiale med organiske molekyler, der kan tilføje til dets elektroniske egenskaber. Kredit:Jingjing Xue og Rui Wang/UCLA Samueli School of Engineering UCLA materialeforsker
- For at holde Saturns En ring indeholdt, dens måner står forenet
- Ny undersøgelse viser, at furfuralderivater er en måde at gøre produktion af vedvarende brændsto…
- Softwareprogrammet Allchemy identificerer præbiotisk syntese af biokemiske forbindelser fra urpræk…
- Ny opdagelse finder, at sultende hvide dværge er spisespisende
- Hvad er Lewis-strukturen for PCI3?
- Fordelene ved simpel destillation


