Hvad vil der ske, hvis der tilføjes en stor mængde NaCl til den vandige opløsning?
1. Øget ionstyrke:
* øget ledningsevne: Opløsningen vil blive mere ledende, når koncentrationen af ioner (Na+ og Cl-) øges.
* skiftede ligevægte: Hvis opløsningen indeholder andre ioniske arter eller reaktioner, der involverer ioner, skifter ligevægten baseret på Le Chateliers princip.
* Ændrede aktivitetskoefficienter: Aktiviteten af ioner i opløsningen vil falde, når deres interaktion med hinanden bliver stærkere på grund af den øgede ionstyrke. Dette kan påvirke reaktionshastigheden og opløseligheden af andre salte.
2. Salting-out-effekt:
* Nedsat opløselighed af ikke -polære molekyler: Tilstedeværelsen af en høj koncentration af saltioner kan reducere opløseligheden af ikke -polære molekyler (som organiske forbindelser) i vand. Dette skyldes, at saltionerne interagerer stærkere med vandmolekyler, hvilket gør dem mindre tilgængelige til at interagere med ikke -polære molekyler.
3. Ændringer i fysiske egenskaber:
* øget densitet: Løsningen af opløsningen vil stige, når koncentrationen af salt øges.
* Nedsat frysepunkt: Opløsningens frysepunkt vil falde (dette er princippet bag salt, der bruges på iskolde veje).
* Øget kogepunkt: Kogepunktet for opløsningen vil stige.
4. Udfældning:
* mulig saltudfældning: Hvis koncentrationen af NaCI overstiger dens opløselighedsgrænse, udfældes noget af saltet ud af opløsningen som faste krystaller.
5. Andre effekter:
* pH -ændringer: Hvis opløsningen ikke er bufret, kan tilsætning af en stor mængde NaCl let reducere pH. Dette skyldes, at hydrolysen af Na+ -ionerne kan producere en lille mængde H+ -ioner.
* Korrosion: Afhængig af de andre komponenter i opløsningen kan høje saltkoncentrationer bidrage til korrosion.
Kortfattet: Tilføjelse af en stor mængde NaCI til en vandig opløsning vil ændre dens fysiske og kemiske egenskaber markant. De nøjagtige effekter afhænger af de oprindelige betingelser for opløsningen, mængden af NaCl tilsat og tilstedeværelsen af andre opløste stoffer.
Sidste artikelHvilken gas indånder vi ud?
Næste artikelHvorfor opvarmes en løsning under fordampning i laboratoriet?
 Varme artikler
Varme artikler
-
 Nøglemekanismer for luftvejsafslapning ved astma afsløret i ny undersøgelseKredit:Pixabay/CC0 Public Domain Mange lægemidler til astma og andre obstruktive lungesygdomme er rettet mod β2 -adrenerg receptor (β2 AR), en G-proteinkoblet receptor (GPCR), der hurtigt understøt
Nøglemekanismer for luftvejsafslapning ved astma afsløret i ny undersøgelseKredit:Pixabay/CC0 Public Domain Mange lægemidler til astma og andre obstruktive lungesygdomme er rettet mod β2 -adrenerg receptor (β2 AR), en G-proteinkoblet receptor (GPCR), der hurtigt understøt -
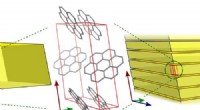 Fluorescerende krystal mysterium løstSkematisk, der viser den ikke-lagdelte krystalstruktur af syntetisk coronen (venstre) og den lagdelte struktur af naturlig karpatit (højre). Begge strukturer blev bestemt gennem røntgenkrystallografi
Fluorescerende krystal mysterium løstSkematisk, der viser den ikke-lagdelte krystalstruktur af syntetisk coronen (venstre) og den lagdelte struktur af naturlig karpatit (højre). Begge strukturer blev bestemt gennem røntgenkrystallografi -
 Forudsige året i kemiKredit:CC0 Public Domain Med 2020 lige begyndt, forskere rundt om i verden undrer sig over, hvad året har i vente for dem. For at hjælpe med at styre dem lige, Kemi- og ingeniørnyheder ( C&EN
Forudsige året i kemiKredit:CC0 Public Domain Med 2020 lige begyndt, forskere rundt om i verden undrer sig over, hvad året har i vente for dem. For at hjælpe med at styre dem lige, Kemi- og ingeniørnyheder ( C&EN -
 Elektrisk fosfatsignatur hjælper med at registrere vigtige cellulære hændelserGrafisk abstrakt. Kredit:Tokyo Tech Hver dag forekommer millioner af biologiske processer i vores krop på cellulært niveau. At studere disse processer kan hjælpe os med at lære mere om, hvordan cel
Elektrisk fosfatsignatur hjælper med at registrere vigtige cellulære hændelserGrafisk abstrakt. Kredit:Tokyo Tech Hver dag forekommer millioner af biologiske processer i vores krop på cellulært niveau. At studere disse processer kan hjælpe os med at lære mere om, hvordan cel
- Brug AI til at opdage landings- og udforskningssteder på månen
- Reverse engineering materialer for mere effektiv opvarmning og køling
- Hvilken rolle spiller antioxidanter i den menneskelige krop og på hjernen specifikt?
- Omformning af vores forståelse af granulære systemer
- Hvis du har en enzymatisk reaktion, der forløber ved den optimale pH og temperatur. Tilføjer du en…
- Brug af maskinlæring til at finjustere visninger af den gamle fortid


