Hvorfor kan flydende koge ved lavt tryk?
forståelse af kogning
* kogepunkt: Kogepunktet for en væske er den temperatur, hvormed dens damptryk er lig med det omgivende atmosfæriske tryk. Dette betyder, at væskens molekyler har nok energi til at flygte ind i gasfasen.
* damptryk: Det tryk, der udøves af dampen af en væske i ligevægt med dens flydende fase. Dette tryk øges, når væsken bliver varmere, fordi molekylerne bevæger sig hurtigere og har en større chance for at flygte ind i gasfasen.
lavere tryk, lavere kogepunkt
* Nedsat modstand: Når det omgivende tryk er lavere, er der mindre modstand for, at væskemolekylerne overvindes for at flygte ind i gasfasen.
* lettere flugt: Tænk på det sådan:Hvis du prøver at skubbe en tung dør op, er det lettere, hvis nogen hjælper dig på den anden side. Et lavere tryk er som at have nogen, der hjælper de flydende molekyler med at flygte.
* når ligevægt: Ved et lavere tryk når væsken sit ligevægtsdamptryk ved en lavere temperatur. Dette betyder, at væsken koger ved en lavere temperatur.
Eksempler:
* Madlavning i høje højder: I højere højder er det atmosfæriske tryk lavere. Dette er grunden til, at vand koger ved en lavere temperatur i bjergene, hvilket gør det sværere at tilberede mad ordentligt.
* vakuumpumper: Vakuumpumper bruges til at skabe miljøer med lavt tryk. Dette er grunden til, at væsker koger ved en meget lavere temperatur i et vakuum, hvilket muliggør processer som frysetørring.
Kortfattet:
Et lavere trykmiljø reducerer modstanden for flydende molekyler til at flygte ind i gasfasen, hvilket giver dem mulighed for at nå deres ligevægtsdamptryk ved en lavere temperatur. Dette er grunden til, at væsker koger ved lavere temperaturer under reduceret tryk.
Sidste artikelHvor mange elektroner ønsker hvert atom?
Næste artikelHvad er den binære forbindelse af ALCL?
 Varme artikler
Varme artikler
-
 Ny teknologi forbedrer brintproduktionenINL-forskere demonstrerede højtydende elektrokemisk brintproduktion ved en lavere temperatur, end det havde været muligt før. Kredit:Idaho National Laboratory Industrielt brint er tættere på at bl
Ny teknologi forbedrer brintproduktionenINL-forskere demonstrerede højtydende elektrokemisk brintproduktion ved en lavere temperatur, end det havde været muligt før. Kredit:Idaho National Laboratory Industrielt brint er tættere på at bl -
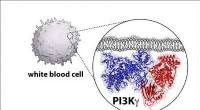 Kemikere udvikler en ny plan for enzym involveret i kræftKredit:University of Oregon Forskere har i årtier vidst, at en bestemt klasse af enzymer er en vigtig aktør inden for cellebiologi, fordi de ofte muterer og bliver væsentlige årsager til kræft. B
Kemikere udvikler en ny plan for enzym involveret i kræftKredit:University of Oregon Forskere har i årtier vidst, at en bestemt klasse af enzymer er en vigtig aktør inden for cellebiologi, fordi de ofte muterer og bliver væsentlige årsager til kræft. B -
 Forskere bygger mikroporøse MOF-fælder til at afbøde giftige gasserKredit:Oak Ridge National Laboratory Nitrogendioxid og svovldioxid (NO2 og SO2 ) er giftige gasser, der er skadelige for miljøet og menneskers sundhed. Når de kommer ind i atmosfæren, kan de rejse
Forskere bygger mikroporøse MOF-fælder til at afbøde giftige gasserKredit:Oak Ridge National Laboratory Nitrogendioxid og svovldioxid (NO2 og SO2 ) er giftige gasser, der er skadelige for miljøet og menneskers sundhed. Når de kommer ind i atmosfæren, kan de rejse -
 Udvikling af cellulær membran-FET (lipid-FET) til følsomhed af biosensorUdfordringer til potentiometriske måleordninger til molekylær detektion på en FET under ionisk miljø:dannelse af EDL, uspecifik binding, og tilfældigt orienterede receptorer. Kredit:Korea Institute of
Udvikling af cellulær membran-FET (lipid-FET) til følsomhed af biosensorUdfordringer til potentiometriske måleordninger til molekylær detektion på en FET under ionisk miljø:dannelse af EDL, uspecifik binding, og tilfældigt orienterede receptorer. Kredit:Korea Institute of
- Hvorfor har jeg forskellige temperaturer på samme tid i dele af verden?
- NASA raketopsendelse vil teste videnskabspakke til fremtidige missioner
- Hvad er funktionen af en snavskop-baffel i vakuum?
- Gamle mus opdaget af klimahulere
- Skovtab i en del af USA kan skade træer på den modsatte kyst
- Påvirker bredden af et gummibånd, hvor langt det vil strække sig?


