Har postulat 4 af Daltons atomteori gældende nu?
Her er hvorfor:
* isotoper: Vi ved nu, at atomer med det samme element kan have forskellige antal neutroner. Disse forskellige former kaldes isotoper. Mens isotoper af det samme element deler det samme antal protoner (og dermed det samme atomnummer), har de forskellige masser på grund af det varierende antal neutroner. Dette modsiger Daltons idé om identisk masse for alle atomer i et element.
* nukleare reaktioner: Daltons teori foregår opdagelsen af nukleare reaktioner. Vi forstår nu, at atomer kan opdeles, smeltes og endda omdannes til andre elementer gennem nukleare processer. Dette viser, at atomer ikke er udelelige, som Dalton troede.
Imidlertid kan Daltons fjerde postulat betragtes som en gyldig tilnærmelse for mange kemiske reaktioner. I de fleste daglige kemiske reaktioner er forskellene i masse og egenskaber mellem isotoper ubetydelige. Atomernes kemiske opførsel bestemmes primært af deres elektronkonfiguration, som stort set bestemmes af antallet af protoner.
Derfor, mens Daltons fjerde postulat ikke er helt nøjagtig, gav det en grundlæggende ramme for udviklingen af moderne atomteori. Det var et betydeligt skridt fremad i vores forståelse af stof, selvom det er blevet raffineret og udvidet.
 Varme artikler
Varme artikler
-
 Enkel enhed overvåger sundhed ved hjælp af svedEn multivalve svedopsamler til overvågning af sundhed. Kredit:Jennifer M. McCann/ Penn State En enhed, der overvåger sundhedsmæssige forhold i kroppen ved hjælp af en persons sved, er udviklet af
Enkel enhed overvåger sundhed ved hjælp af svedEn multivalve svedopsamler til overvågning af sundhed. Kredit:Jennifer M. McCann/ Penn State En enhed, der overvåger sundhedsmæssige forhold i kroppen ved hjælp af en persons sved, er udviklet af -
 Kemikere opdager ny reaktivitet af anstrengte molekylerMünster-teamet bruger denne laboratorieopsætning til at udføre fotocykloaddition. Kredit:University of Münster - Roman Kleinmans I syntetisk organisk kemi er såkaldte cycloadditioner en særlig vigt
Kemikere opdager ny reaktivitet af anstrengte molekylerMünster-teamet bruger denne laboratorieopsætning til at udføre fotocykloaddition. Kredit:University of Münster - Roman Kleinmans I syntetisk organisk kemi er såkaldte cycloadditioner en særlig vigt -
 3-D-printet smart gel ændrer form, når den udsættes for lysDenne blæksprutte har farveskiftende celler, kaldet kromatoforer, i sin hud, et fænomen, der inspirerede Rutgers ingeniører. Kredit:NOAA Okeanos Explorer Program, Galapagos Rift Expedition 2011 In
3-D-printet smart gel ændrer form, når den udsættes for lysDenne blæksprutte har farveskiftende celler, kaldet kromatoforer, i sin hud, et fænomen, der inspirerede Rutgers ingeniører. Kredit:NOAA Okeanos Explorer Program, Galapagos Rift Expedition 2011 In -
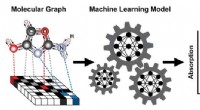 Forudsigelse af røntgenabsorptionsspektre fra graferEt skema, der viser trinene til træning af en maskinlæringsmodel til at forudsige et røntgenabsorptionsspektrum (XAS) baseret på den kendte struktur af et molekyle. Molekylets struktur er repræsentere
Forudsigelse af røntgenabsorptionsspektre fra graferEt skema, der viser trinene til træning af en maskinlæringsmodel til at forudsige et røntgenabsorptionsspektrum (XAS) baseret på den kendte struktur af et molekyle. Molekylets struktur er repræsentere
- Hvilken kraft får en snebold, der ruller ned ad den græsklædte bakke, til at bremse eller acceler…
- Narkotikatests for spillere, efterhånden som eWorld Cup-jackpotten stiger
- Hvad er de fire hovedmetoder til fremstilling af ATP?
- Det er en verdensomspændende udfordring at demonstrere forskningens indvirkning på samfundet
- Kræver natrium-kalium-pumpen energi for at fungere?
- Hvordan kan vand gå fra jord til toppen af et træ?


