Hvad ændrer enzymer ved en kemisk reaktion?
1. Sænkning af aktiveringsenergien:
* Hvad er aktiveringsenergi? Det er den mindste mængde energi, der kræves for at en reaktion kan forekomme. Forestil dig en bold, der har brug for at rulle over en bakke for at komme til et lavere punkt. Bakken repræsenterer aktiveringsenergien.
* hvordan enzymer hjælper: Enzymer tilvejebringer en alternativ vej til, at reaktionen kan finde sted, en der har en lavere aktiveringsenergi. Dette betyder, at der er behov for mindre energi til, at reaktionen skal starte, hvilket får den til at ske hurtigere.
2. Tilvejebringelse af et specifikt bindingssted:
* det aktive sted: Enzymer har et specifikt område kaldet det aktive sted, hvor reaktantmolekylerne (kaldet substrater) binder.
* lås og nøglemodel: Dette aktive sted er formet som en lås, og underlaget er som en nøgle. Kun det korrekte underlag kan passe ind på det aktive sted. Denne specificitet sikrer, at enzymet katalyserer den rigtige reaktion.
* induceret fit -model: Det aktive sted kan også ændre form lidt, så den passer bedre til underlaget, hvilket yderligere forbedrer reaktionen.
3. At bringe reaktanter sammen:
* Nærhedseffekt: Enzymer bringer reaktantmolekylerne sammen i den korrekte orientering, hvilket gør det lettere for dem at interagere og danne produkter.
I resumé ændrer enzymer ikke ligevægt af en reaktion (de får ikke noget til at ske, der ikke ville ske ellers). De får simpelthen reaktionen til at ske meget hurtigere af:
* sænkning af den aktiveringsenergi, der kræves for, at reaktionen starter.
* leverer et specifikt bindingssted for reaktanterne.
* samler reaktanterne i den rigtige orientering.
Sidste artikelHvilket element der har en atommasse på 207?
Næste artikelHvad er eksempel på en hydroxylgruppe?
 Varme artikler
Varme artikler
-
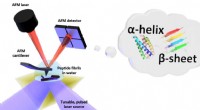 Formen i vand:Første nanoskalamålinger af biomolekylefoldning i væskeSkematisk af opsætningen for fototermisk induceret resonans (PTIR), som inkluderer en infrarød laserkilde og atomic force microscope (AFM) cantilever med en skarp spids, der rører prøven og vibrerer s
Formen i vand:Første nanoskalamålinger af biomolekylefoldning i væskeSkematisk af opsætningen for fototermisk induceret resonans (PTIR), som inkluderer en infrarød laserkilde og atomic force microscope (AFM) cantilever med en skarp spids, der rører prøven og vibrerer s -
 Kemikalier af høj værdi til lægemidler kan gøres billigere og grønnere af nye katalysatorerForskere fra venstre mod højre:Jonathan Barrios-Rivera, Martin Wills, Yingjian Xu. Kredit:University of Warwick Kemikalier af høj værdi, der bruges til at fremstille lægemidler, kunne gøres meget
Kemikalier af høj værdi til lægemidler kan gøres billigere og grønnere af nye katalysatorerForskere fra venstre mod højre:Jonathan Barrios-Rivera, Martin Wills, Yingjian Xu. Kredit:University of Warwick Kemikalier af høj værdi, der bruges til at fremstille lægemidler, kunne gøres meget -
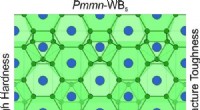 Forskere forudser et nyt superhårdt materiale med unikke egenskaberKredit:The Journal of Physical Chemistry Letters Et internationalt hold af forskere har rapporteret om et nyt superhårdt materiale, der kunne bruges til boring, maskinbygning og andre områder. D
Forskere forudser et nyt superhårdt materiale med unikke egenskaberKredit:The Journal of Physical Chemistry Letters Et internationalt hold af forskere har rapporteret om et nyt superhårdt materiale, der kunne bruges til boring, maskinbygning og andre områder. D -
 Undervurderet kemisk mangfoldighedKredit:CC0 Public Domain Sidste gang der blev udarbejdet en liste over alle de kemikalier, der er tilgængelige på markedet og i omløb verden over, det løb til 100, 000 poster. Udarbejdet kort efte
Undervurderet kemisk mangfoldighedKredit:CC0 Public Domain Sidste gang der blev udarbejdet en liste over alle de kemikalier, der er tilgængelige på markedet og i omløb verden over, det løb til 100, 000 poster. Udarbejdet kort efte
- Laboratorieforsøg viser, at halvleder nanotråde kan tunes over brede energiområder
- Størrelsen bestemmer, hvordan nanopartikler påvirker biologiske membraner
- Californien går glip af milliarder af liter regnvand hvert år, viser rapporten
- Sådan beregnes en fraktion Covalent
- En dæmning lige over Vesterhavet
- Hvilket lag udfører fotosyntesen?


