Hvad er eksempel på en hydroxylgruppe?
enkle eksempler:
* vand (H2O): To hydrogenatomer er bundet til et iltatom, der danner en hydroxylgruppe.
* methanol (CH3OH): En methylgruppe (CH3) er bundet til en hydroxylgruppe.
* ethanol (C2H5OH): En ethylgruppe (C2H5) er bundet til en hydroxylgruppe.
mere komplekse eksempler:
* sukker (f.eks. Glukose, fruktose): Sukkerarter indeholder flere hydroxylgrupper.
* alkoholer (f.eks. Methanol, ethanol, isopropanol): Det afgørende træk ved alkoholer er tilstedeværelsen af en eller flere hydroxylgrupper.
* aminosyrer (f.eks. Serin, threonin): Nogle aminosyrer indeholder en hydroxylgruppe fastgjort til deres sidekæder.
* phenoler (f.eks. Phenol, cresol): Disse aromatiske forbindelser indeholder en hydroxylgruppe, der er direkte fastgjort til en aromatisk ring.
* carboxylsyrer (f.eks. eddikesyre, mælkesyre): Selvom det ikke er teknisk en hydroxylgruppe, har carboxylsyrer en carboxylgruppe (-COOH), der inkluderer en hydroxylgruppe.
Vigtig note: Tilstedeværelsen af en hydroxylgruppe kan væsentligt påvirke egenskaberne ved et molekyle. Det kan bidrage til:
* Øget polaritet: Hydroxylgrupper er polære på grund af det elektronegative iltatom. Dette kan øge opløseligheden af et molekyle i vand.
* Hydrogenbinding: Hydroxylgrupper kan danne hydrogenbindinger med andre molekyler, hvilket bidrager til intermolekylære interaktioner og egenskaber som kogepunkt.
* Kemisk reaktivitet: Hydroxylgruppen kan deltage i forskellige kemiske reaktioner, såsom dehydreringsreaktioner eller oxidationsreaktioner.
Sidste artikelHvad ændrer enzymer ved en kemisk reaktion?
Næste artikelHvad afhænger PH af vand af antallet af?
 Varme artikler
Varme artikler
-
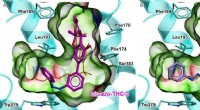 Berusende lysfølsommeTo lysfølsomme THC -derivater, og hvordan de er indlejret i cannabinoidreceptoren 1. Kredit:fra Westphal MV et al. J. Am. Chemical Soc., 2017, 139 (50), s. 18206-18212. ETH -kemikere har syntetise
Berusende lysfølsommeTo lysfølsomme THC -derivater, og hvordan de er indlejret i cannabinoidreceptoren 1. Kredit:fra Westphal MV et al. J. Am. Chemical Soc., 2017, 139 (50), s. 18206-18212. ETH -kemikere har syntetise -
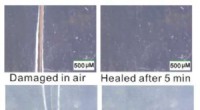 Forskere opdager ny type selvhelbredende materialeØverste panel:Optiske mikroskopbilleder af beskadigede (venstre) og reparerede (højre) prøver af et af materialerne i luft ved 25 °C. En film blev knækket af et barberblad og derefter efterladt i luft
Forskere opdager ny type selvhelbredende materialeØverste panel:Optiske mikroskopbilleder af beskadigede (venstre) og reparerede (højre) prøver af et af materialerne i luft ved 25 °C. En film blev knækket af et barberblad og derefter efterladt i luft -
 Origami inspirerer til ny teknologi til vævsregenereringUMass Lowell Prof. Gulden Camci-Unal arbejder sammen med studerende Xinchen Wu om biomaterialeforskning ved universitetets Saab Emerging Technologies and Innovation Center. Kredit:Edwin Aguirre for UM
Origami inspirerer til ny teknologi til vævsregenereringUMass Lowell Prof. Gulden Camci-Unal arbejder sammen med studerende Xinchen Wu om biomaterialeforskning ved universitetets Saab Emerging Technologies and Innovation Center. Kredit:Edwin Aguirre for UM -
 En opfindelse muliggør fremstilling af et naturligt sødemiddelKredit:Universitetet i Oulu En forskergruppe fra Oulu Universitet har udviklet en metode, der er i stand til at fremstille det naturlige sødestof brazzein. Produktion af brazzein som et velsmagend
En opfindelse muliggør fremstilling af et naturligt sødemiddelKredit:Universitetet i Oulu En forskergruppe fra Oulu Universitet har udviklet en metode, der er i stand til at fremstille det naturlige sødestof brazzein. Produktion af brazzein som et velsmagend
- Fysikere måler van der Waals kræfter fra individuelle atomer for første gang
- Hvordan de engelske optøjer i 2011 spredte sig - nye beviser viser, at identitetsfølelse var nøgl…
- Stor risiko, forankrede interesser og Trumps tilbagerulning af miljøregler
- Hvor meget er 100 fod i diameter i meter?
- Videnskab Transport Aktiviteter til førskolebørn
- Nødvendighed er virkelig opfindelsens moder - uanset ressourcer, undersøgelse viser


