Hvad er elementerne i gruppe to af periodisk tabel?
* beryllium (BE)
* magnesium (mg)
* calcium (CA)
* strontium (SR)
* barium (BA)
* radium (RA)
Disse elementer deler flere almindelige egenskaber, herunder:
* Høj reaktivitet: De er alle reaktive metaller, selvom de er mindre reaktive end alkalimetaller (gruppe 1).
* to valenselektroner: De har to elektroner i deres yderste skal, hvilket får dem til let at danne ioniske bindinger ved at miste disse elektroner.
* Formalkaliske oxider: Når de reagerer med ilt, danner de oxider, der er alkaliske (basale), når de opløstes i vand.
* blød og sølvfarvet: De er bløde metaller med et sølvfarvet hvidt udseende.
* gode ledere af varme og elektricitet: De er gode ledere af varme og elektricitet.
Fortæl mig, hvis du gerne vil lære mere om ethvert specifikt alkalisk jordmetal!
Sidste artikelIndsamlingspunkt for forbindelser, der skal udskilles, er?
Næste artikelHvorfor er ozon en stabil allotrop af ilt?
 Varme artikler
Varme artikler
-
 Lyser på et obskurt proteomKredit:Unsplash/CC0 Public Domain Massespektrometri baseret proteomik er big-data videnskaben om proteiner, der tillader overvågning af overfloden af tusindvis af proteiner i en prøve på én gang.
Lyser på et obskurt proteomKredit:Unsplash/CC0 Public Domain Massespektrometri baseret proteomik er big-data videnskaben om proteiner, der tillader overvågning af overfloden af tusindvis af proteiner i en prøve på én gang. -
 En 3-D tilgang til at stoppe kræft i sine sporKræftceller er traditionelt blevet undersøgt i petriskåle og på objektglas. Forskere har nu udviklet en 3D-model til at analysere kompleksiteten af kræftceller i et miljø, der i højere grad efterlig
En 3-D tilgang til at stoppe kræft i sine sporKræftceller er traditionelt blevet undersøgt i petriskåle og på objektglas. Forskere har nu udviklet en 3D-model til at analysere kompleksiteten af kræftceller i et miljø, der i højere grad efterlig -
 Parfumemagere søger naturligt, bæredygtige dufteKredit:CC0 Public Domain I 1921, parfumeur Ernest Beaux opdagede, at tilføjelse af syntetiske aldehyder til naturlige rose- og jasmindufte producerede den helt rigtige duftkombination til den ikon
Parfumemagere søger naturligt, bæredygtige dufteKredit:CC0 Public Domain I 1921, parfumeur Ernest Beaux opdagede, at tilføjelse af syntetiske aldehyder til naturlige rose- og jasmindufte producerede den helt rigtige duftkombination til den ikon -
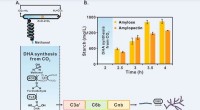 Kinesiske videnskabsmænd rapporterer om stivelsesyntese fra kuldioxidStivelsessyntese via kunstig stivelse anabolsk vej (ASAP) fra kuldioxid. Kredit:TIBCAS Kinesiske videnskabsmænd rapporterede for nylig om en de novo-rute til kunstig stivelsessyntese fra kuldioxid
Kinesiske videnskabsmænd rapporterer om stivelsesyntese fra kuldioxidStivelsessyntese via kunstig stivelse anabolsk vej (ASAP) fra kuldioxid. Kredit:TIBCAS Kinesiske videnskabsmænd rapporterede for nylig om en de novo-rute til kunstig stivelsessyntese fra kuldioxid
- Ung åben klynge NGC 602 inspiceret med ALMA
- Australsk politi jager morder af kæmpe krokodille
- Et skridt tættere på praktisk solbrintproduktion via kunstfærdigt modificeret hæmatitfotoanode
- Team programmerer en humanoid robot til at kommunikere på tegnsprog
- Påvirker mængden af vandhøjde en ærteplante?
- Udskrivning af et bedre mikronet


