Hvad sker der, når NAC1 tilsættes til vand?
opløsning:
1. ionisering: De stærke ioniske bindinger, der holder natrium (Na+) og chlorid (Cl-) ioner sammen i NaCl-krystalgitteret, forstyrres af de polære vandmolekyler.
2. Hydrering: Den positive ende af vandmolekylet (brint) tiltrækkes af de negativt ladede chloridioner (Cl-), mens den negative ende af vandmolekylet (ilt) tiltrækkes af de positivt ladede natriumioner (Na+). Denne attraktion danner hydrationsskaller omkring ionerne og trækker dem effektivt fra krystalgitteret.
3. dissociation: Efterhånden som hydratiseringsprocessen fortsætter, bliver Na+ og klorerne fuldstændigt omgivet af vandmolekyler, der adskiller dem fra hinanden og giver dem mulighed for at bevæge sig frit i opløsningen. Denne proces kaldes dissociation.
Resultat:
* NaCl opløses i vand og danner en homogen opløsning.
* Opløsningen udfører elektricitet på grund af tilstedeværelsen af frie ioner (Na+ og Cl-).
* Vandet bliver lidt salt.
Vigtig note:
* Opløsningsprocessen er en endotermisk reaktion, hvilket betyder, at den absorberer varme fra omgivelserne. Dette er grunden til at tilføje salt til vand kan sænke frysepunktet og hæve kogepunktet.
* Ikke alle salte opløses i vand i samme omfang. Opløseligheden af et salt afhænger af faktorer såsom temperatur, styrken af de ioniske bindinger og polariteten af opløsningsmidlet.
Sidste artikelHvad bliver Phyllite til?
Næste artikelHvad er årsagerne til surhed i normalt regnvand?
 Varme artikler
Varme artikler
-
 Undersøgelse afslører, hvordan et lille molekyle fremmer fjernelse af overskydende kolesterolEt lille molekyle (vist her i pink) med evnen til at øge godt (HDL) kolesterol i dyremodeller binder sig til det membranbindende domæne af lecithin:kolesterol acyltransferase (LCAT; vist i blågrøn). S
Undersøgelse afslører, hvordan et lille molekyle fremmer fjernelse af overskydende kolesterolEt lille molekyle (vist her i pink) med evnen til at øge godt (HDL) kolesterol i dyremodeller binder sig til det membranbindende domæne af lecithin:kolesterol acyltransferase (LCAT; vist i blågrøn). S -
 Nye fingeraftryk tilføjet til kemisk identifikationsdatabaseNIST -forskningskemiker Kelly Telu injicerer en prøve i et massespektrometer, et laboratorieinstrument, som forskere bruger til at identificere ukendte kemiske forbindelser. Kredit:M. Delorme/NIST
Nye fingeraftryk tilføjet til kemisk identifikationsdatabaseNIST -forskningskemiker Kelly Telu injicerer en prøve i et massespektrometer, et laboratorieinstrument, som forskere bruger til at identificere ukendte kemiske forbindelser. Kredit:M. Delorme/NIST -
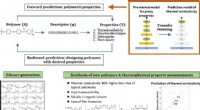 Succesfuld anvendelse af maskinlæring i opdagelsen af nye polymererKredit:Tokyo Tech En fælles forskergruppe, herunder Ryo Yoshida (professor og direktør for Data Science Center for Creative Design and Manufacturing ved Institute of Statistical Mathematics [ISM],
Succesfuld anvendelse af maskinlæring i opdagelsen af nye polymererKredit:Tokyo Tech En fælles forskergruppe, herunder Ryo Yoshida (professor og direktør for Data Science Center for Creative Design and Manufacturing ved Institute of Statistical Mathematics [ISM], -
 Belysning af stien for cellerNeuroner følger det kortlagte mønster i en hydrogel. Kredit:ETH Zürich ETH -forskere har udviklet en ny metode, hvor de bruger lys til at tegne mønstre af molekyler, der styrer levende celler. Fre
Belysning af stien for cellerNeuroner følger det kortlagte mønster i en hydrogel. Kredit:ETH Zürich ETH -forskere har udviklet en ny metode, hvor de bruger lys til at tegne mønstre af molekyler, der styrer levende celler. Fre
- Smeltende små gletschere kunne føje 10 tommer til havniveauet
- Hyperspektral opløsning stimuleret Raman-spektroskopi med forstærkede fs-pulsudbrud
- Hvad er 31,6 grader Celsius i Fahrenheit?
- Hvor er min pakke? Almindelige fragtskabe kan lette bytrafikken og forhindre mislykkede leverancer
- Forskere identificerer ny metode til at øge laserbehandlingsopløsningen
- Moderne mennesker opstod mere end 300, 000 år siden, ny undersøgelse tyder på


