Hvorfor danner lipid -dobbeltlag spontant?
1. Hydrofob effekt:
* Lipider er amfipatiske molekyler, hvilket betyder, at de har både hydrofile (vandelskende) og hydrofobe (vandfryd) regioner.
* De hydrofobe haler af phospholipider, som typisk er sammensat af fedtsyrekæder, afvises af vand.
* For at minimere kontakten med vand forbinder disse hydrofobe haler med hinanden og danner en kerne i dobbeltlaget.
2. Entropi:
* Dannelsen af et dobbeltlag øger systemets entropi. Dette skyldes, at vandmolekylerne, der tidligere blev bestilt omkring de hydrofobe haler af lipiderne, bliver mere forstyrrede, når lipiderne forbinder hinanden.
* Denne stigning i entropi er en termodynamisk gunstig proces.
3. Van der Waals -interaktioner:
* Svage van der Waals -kræfter findes mellem de hydrofobe haler af phospholipiderne, hvilket hjælper med at stabilisere dobbeltlagsstrukturen.
4. Elektrostatiske interaktioner:
* De hydrofile hoveder af phospholipiderne interagerer med de omgivende vandmolekyler via elektrostatiske interaktioner, hvilket yderligere stabiliserer dobbeltlagsstrukturen.
5. Minimering af overfladeareal:
* Dannelsen af et dobbeltlag minimerer det overfladeareal, der udsættes for vand, hvilket er energisk gunstigt.
6. Selvmontering:
* Evnen til lipidmolekyler til at samles i dobbeltlag er et resultat af deres iboende kemiske egenskaber og det omgivende miljø. Denne selvmonteringsproces kræver ikke nogen ekstern energiindgang.
Kortfattet:
Den spontane dannelse af lipid -dobbeltlag drives af en kombination af hydrofobe interaktioner, entropiske overvejelser, van der Waals -kræfter, elektrostatiske interaktioner og minimering af overfladeareal. Denne proces er termodynamisk gunstig og bidrager væsentligt til dannelsen af cellemembraner og andre biologiske strukturer.
Sidste artikelEr NAC2H3O2 og HCH3O2 en buffer i vand?
Næste artikelEn oxyanion er et eller flere iltatomer bundet til at gøre hvad?
 Varme artikler
Varme artikler
-
 En måde at øge strukturel stabilitet i anstrengte halogenidperovskitteren, Optiske billeder af de voksende epitaksiale α-FAPbI3 tynde film. Den høje gennemsigtighed af substraterne og de glatte overflader af de tynde film demonstrerer deres høje kvalitet. Målestænger, 4
En måde at øge strukturel stabilitet i anstrengte halogenidperovskitteren, Optiske billeder af de voksende epitaksiale α-FAPbI3 tynde film. Den høje gennemsigtighed af substraterne og de glatte overflader af de tynde film demonstrerer deres høje kvalitet. Målestænger, 4 -
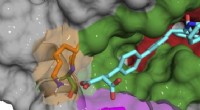 Ny strategi til præcist at målrette undertyper af nøgleproteinRøntgen-co-krystalstruktur af B52-forbindelse (cyan), der binder og hæmmer cyclophilin D-protein. Kredit:Aziz Rangwala Cyclosporin er et af de mest almindelige og effektive immunsuppressive lægemid
Ny strategi til præcist at målrette undertyper af nøgleproteinRøntgen-co-krystalstruktur af B52-forbindelse (cyan), der binder og hæmmer cyclophilin D-protein. Kredit:Aziz Rangwala Cyclosporin er et af de mest almindelige og effektive immunsuppressive lægemid -
 Ny schweizisk hærkniv renser for vandforureningMedforfatterne Vinayak Dravid og Stephanie Ribet undersøger deres fosfateliminerings- og genvindingssubstrat. Kredit:Northwestern University Fosfatforurening i floder, søer og andre vandveje har n
Ny schweizisk hærkniv renser for vandforureningMedforfatterne Vinayak Dravid og Stephanie Ribet undersøger deres fosfateliminerings- og genvindingssubstrat. Kredit:Northwestern University Fosfatforurening i floder, søer og andre vandveje har n -
 Litauere udvikler en takeaway-madpakke, der er fuldstændig plastikfriKaunas borgere, forskere og virksomheder skabte en innovativ madpakke med madpakke under en fælles workshop. Kredit:KTU Takeaway mad er blevet en integreret del af vores liv. På trods af bekvemmeli
Litauere udvikler en takeaway-madpakke, der er fuldstændig plastikfriKaunas borgere, forskere og virksomheder skabte en innovativ madpakke med madpakke under en fælles workshop. Kredit:KTU Takeaway mad er blevet en integreret del af vores liv. På trods af bekvemmeli
- Hvad er en væske, der opvarmes, kan kaldes?
- Hvordan partipolitisk kunne tage en bid af din pengepung
- At give naturen juridisk personskab er en voksende bevægelse:Kan det dæmme op for tab af biodivers…
- Hvordan påvirker Jordens indre kerne seismiske bølger?
- Hvad sker der, når et kompas bringes tættere på magneten?
- Uddybende spørgsmål:Hvad opvarmer jordens kerne?


