Hvad er den mest inerte form for kulstof?
Her er hvorfor:
* stærke kovalente obligationer: Diamonds struktur består af et stift, tredimensionelt netværk af carbonatomer bundet til fire andre carbonatomer af stærke kovalente bindinger. Disse bindinger er meget vanskelige at bryde, hvilket gør diamanten ekstremt stabil og resistent over for kemiske reaktioner.
* højt smeltepunkt: Diamond har det højeste smeltepunkt for ethvert element, hvilket yderligere understreger dets stærke binding og stabilitet.
* uopløselig: Diamond er uopløselig i de fleste opløsningsmidler, inklusive vand og syrer.
Mens andre former for kulstof, som grafit, også er temmelig inerte, gør Diamonds usædvanligt stærke kovalente bindinger det mest inerte.
 Varme artikler
Varme artikler
-
 Ny metode fremskynder udviklingen af medicinI laboratoriet hos Bernhard Spingler (r.), praktikant Philipp Nievergelt (l.) ydede et vigtigt bidrag til hurtigere og lettere at bestemme krystalstrukturerne af organiske salte. Kredit:UZH Forske
Ny metode fremskynder udviklingen af medicinI laboratoriet hos Bernhard Spingler (r.), praktikant Philipp Nievergelt (l.) ydede et vigtigt bidrag til hurtigere og lettere at bestemme krystalstrukturerne af organiske salte. Kredit:UZH Forske -
 Forskere finder en ny forbindelse mellem cellemetabolisme og celledelingKredit:CC0 Public Domain Processerne i levende væsener følger en fint orkestreret koreografi ned på molekylært niveau. Rytmiske processer findes overalt i biologien, for eksempel, døgnets døgncykl
Forskere finder en ny forbindelse mellem cellemetabolisme og celledelingKredit:CC0 Public Domain Processerne i levende væsener følger en fint orkestreret koreografi ned på molekylært niveau. Rytmiske processer findes overalt i biologien, for eksempel, døgnets døgncykl -
 Neutroner kaster lys over industriel katalysator til brintproduktionSamarbejdspartnere ved Department of Energys Oak Ridge National Laboratory og amerikanske universiteter brugte neutronspredning og andre avancerede karakteriseringsteknikker til at studere, hvordan en
Neutroner kaster lys over industriel katalysator til brintproduktionSamarbejdspartnere ved Department of Energys Oak Ridge National Laboratory og amerikanske universiteter brugte neutronspredning og andre avancerede karakteriseringsteknikker til at studere, hvordan en -
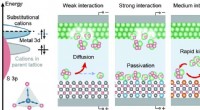 Vulkanformet trend muliggør rationelt design af polysulfidkatalysatorer i lithium-svovlbatterierSkematisk diagram af designprincipper for højeffektive lithium-svovl-katalysatorer. Kredit:Shen Zihan Et fælles forskerhold ledet af prof. Zhang Huigang fra Institute of Process Engineering (IPE) v
Vulkanformet trend muliggør rationelt design af polysulfidkatalysatorer i lithium-svovlbatterierSkematisk diagram af designprincipper for højeffektive lithium-svovl-katalysatorer. Kredit:Shen Zihan Et fælles forskerhold ledet af prof. Zhang Huigang fra Institute of Process Engineering (IPE) v


