Hvad sker der med et opløseligt fast stof, når det tilsættes vand?
1. opløsning: De faste partikler opdeles i individuelle ioner eller molekyler og bliver omgivet af vandmolekyler. Denne proces kaldes opløsning . Vandmolekylerne danner A hydreringsskal Omkring ioner eller molekyler, som hjælper med at adskille dem fra hinanden og holde dem opløst.
2. Dannelse af en løsning: De opløste faste partikler er nu jævnt fordelt over vandet og danner en homogen blanding kaldes en løsning . Vandet er opløsningsmiddel og det opløste fast stof er opløstende .
3. Dynamisk ligevægt: Opløsningsprocessen er ofte en reversibel reaktion. Dette betyder, at nogle af de opløste faste partikler også kan krystallisere og vende tilbage til fast tilstand. Hastigheden for opløsning og krystallisation når en balance, hvilket fører til en dynamisk ligevægt .
Faktorer, der påvirker opløselighed:
* Temperatur: Opløselighed af de fleste faste stoffer øges med temperaturen.
* tryk: Trykket har ringe indflydelse på opløseligheden af faste stoffer.
* Natur af opløst stof og opløsningsmiddel: Polariteten af opløst stof og opløsningsmiddel spiller en betydelig rolle i opløselighed. "Som opløser som"-polære opløste stoffer opløses i polære opløsningsmidler, og ikke-polære opløste stoffer opløses i ikke-polære opløsningsmidler.
Eksempler på opløselige faste stoffer:
* Sukker
* Salt
* Bagepulver
* Kaliumpermanganat
Bemærk: Nogle faste stoffer er kun lidt opløselige i vand, mens andre er meget opløselige. Omfanget af opløselighed afhænger af det specifikke faste stof og betingelserne.
 Varme artikler
Varme artikler
-
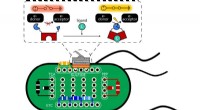 Switch-in-a-celle elektrificerer livetRice University forskere brugte E coli bakterier som en platform til at teste proteinkontakter, der kan bruges til at kontrollere strømmen af elektroner. Proteiner placeret i celler kan simpelthen
Switch-in-a-celle elektrificerer livetRice University forskere brugte E coli bakterier som en platform til at teste proteinkontakter, der kan bruges til at kontrollere strømmen af elektroner. Proteiner placeret i celler kan simpelthen -
 Hjemme-COVID-19-test:Hvor gode er de?Kredit:Pixabay/CC0 Public Domain Da landet bliver vaccineret og begynder at genåbne, test er stadig et centralt element i sikre interaktioner. Hurtig test for COVID-19 er blevet mere almindelig og
Hjemme-COVID-19-test:Hvor gode er de?Kredit:Pixabay/CC0 Public Domain Da landet bliver vaccineret og begynder at genåbne, test er stadig et centralt element i sikre interaktioner. Hurtig test for COVID-19 er blevet mere almindelig og -
 Bredere applikationer til udkogning af en ægmaskineProfessor Colin Raston, professor i ren teknologi, College of Science and Engineering. Kredit:Flinders University Bredere rene kemi -applikationer af den ekstraordinære Vortex Fluidic Device - opf
Bredere applikationer til udkogning af en ægmaskineProfessor Colin Raston, professor i ren teknologi, College of Science and Engineering. Kredit:Flinders University Bredere rene kemi -applikationer af den ekstraordinære Vortex Fluidic Device - opf -
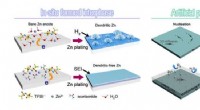 Grænsefladekemi forbedrer genopladeligheden af Zn-batterierIn situ dannede og kunstige beskyttende interfaser for at tæmme Zn elektrokemi. Kredit:ZHAO Jingwen, ZHAO Zhiming og QIU Huayu Med stor interesse for miljøvenlig og effektiv ressourceudnyttelse, g
Grænsefladekemi forbedrer genopladeligheden af Zn-batterierIn situ dannede og kunstige beskyttende interfaser for at tæmme Zn elektrokemi. Kredit:ZHAO Jingwen, ZHAO Zhiming og QIU Huayu Med stor interesse for miljøvenlig og effektiv ressourceudnyttelse, g
- Hvordan gør træer kuldioxid til ilt?
- Chrome-beskrivelser af billeder vil give fingerpeg for blinde og svagsynede brugere
- Klimaændringer er allerede ved at omforme PNW-kyster:Stammelande viser, hvordan man tilpasser sig
- Kalorieindslag på menuer forårsager flere sundhedsomtaler i online restaurantanmeldelser
- Japansk ekspedition identificerer smeltende hotspot i Østantarktis
- Honolulus borgmester nedlægger veto mod lovforslaget om at begrænse Uber, Lyft surge takster


