Hvilke egenskaber kan hjælpe dig med at bestemme, om et stof er molekylært eller ionisk?
Fysiske egenskaber:
* smeltepunkt og kogepunkt:
* ioniske forbindelser generelt har høje smeltnings- og kogepunkter Fordi de stærke elektrostatiske kræfter mellem ioner kræver en masse energi for at bryde.
* molekylære forbindelser har typisk lavere smelte- og kogepunkter Fordi de svagere intermolekylære kræfter (som van der Waals kræfter eller hydrogenbinding) mellem molekyler kræver mindre energi for at overvinde.
* opløselighed:
* ioniske forbindelser er normalt opløselige i polære opløsningsmidler Som vand, fordi de polære vandmolekyler kan omringe og interagere med de ladede ioner og trække dem fra hinanden.
* molekylære forbindelser har tendens til at være opløselig i ikke -polære opløsningsmidler Som hexan eller benzen, fordi de kan interagere med lignende ikke -polære molekyler gennem svage intermolekylære kræfter.
* Konduktivitet:
* ioniske forbindelser I deres smeltede tilstand eller opløst i vand er gode ledere af elektricitet Fordi de mobile ioner kan bære elektrisk strøm.
* molekylære forbindelser er typisk dårlige ledere af elektricitet Fordi de mangler frit bevægende ladede partikler.
* tilstand ved stuetemperatur:
* ioniske forbindelser er normalt faste stoffer ved stuetemperatur På grund af de stærke elektrostatiske kræfter mellem ioner.
* molekylære forbindelser Kan være faste stoffer, væsker eller gasser ved stuetemperatur Afhængig af styrken af deres intermolekylære kræfter.
Kemiske egenskaber:
* dannelse:
* ioniske forbindelser Form typisk mellem metaller og ikke -metaller På grund af overførsel af elektroner.
* molekylære forbindelser Form typisk mellem ikke -metaller gennem deling af elektroner.
Andre ledetråde:
* Formel:
* ioniske forbindelser Inddrag ofte en metalkation og en ikke -metal anion (f.eks. NaCl, Cao).
* molekylære forbindelser består typisk af to eller flere ikke -metaller (f.eks. CO2, H2O).
Vigtig note: Det er vigtigt at huske, at dette er generelle tendenser, og der er undtagelser. Nogle molekylære forbindelser kan have høje smeltepunkter, og nogle ioniske forbindelser kan være opløselige i ikke -polære opløsningsmidler. Det er bedst at overveje alle de tilgængelige oplysninger, når man bestemmer, om et stof er ionisk eller molekylært.
Sidste artikelHvad betyder H2SO4 i den periodiske tabel?
Næste artikelHvordan ville man lave 2 m opløsning af en forbindelse?
 Varme artikler
Varme artikler
-
 Billeddannelse på atomniveau kunne tilbyde en køreplan for metaller med nye egenskaberDenne skematiske illustration af den nye palladiumholdige højentropi tillader viser, hvordan ny legering indeholder store palladiumklynger (blå atomer). Kredit:Ting Zhu Højentropi legeringer, som
Billeddannelse på atomniveau kunne tilbyde en køreplan for metaller med nye egenskaberDenne skematiske illustration af den nye palladiumholdige højentropi tillader viser, hvordan ny legering indeholder store palladiumklynger (blå atomer). Kredit:Ting Zhu Højentropi legeringer, som -
 Ny forståelse af kondensering kan føre til en bedre kraftværkskondensator, afisningsmaterialerKandidatstuderende Hyeongyun Cha, postdoc-forsker Soumyadip Sett, professor Nenad Miljkovic og bachelorstuderende Stephen Bosch udfordrer en ældgammel teori om de processer, der styrer rensningen af
Ny forståelse af kondensering kan føre til en bedre kraftværkskondensator, afisningsmaterialerKandidatstuderende Hyeongyun Cha, postdoc-forsker Soumyadip Sett, professor Nenad Miljkovic og bachelorstuderende Stephen Bosch udfordrer en ældgammel teori om de processer, der styrer rensningen af -
 Modifikation af aminosyrer giver nyt udgangspunkt for udvikling af medicinske behandlingerSyntetisk modificerede aminosyrer udgør udgangspunktet for ny medicin. Kredit:University of Bristol Aminosyrer er byggestenene i proteiner, og kemisk modificering af aminosyrer gør det muligt for
Modifikation af aminosyrer giver nyt udgangspunkt for udvikling af medicinske behandlingerSyntetisk modificerede aminosyrer udgør udgangspunktet for ny medicin. Kredit:University of Bristol Aminosyrer er byggestenene i proteiner, og kemisk modificering af aminosyrer gør det muligt for -
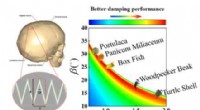 Forholdet mellem sart suturstruktur og dæmpning af biomaterialerFigur 1. De teoretiske modelforudsigelser tyder på, at suturstrukturer fundet i en række naturlige manifestationer har udviklet sig til deres optimale geometrier for at opnå den bedste dæmpningsydelse
Forholdet mellem sart suturstruktur og dæmpning af biomaterialerFigur 1. De teoretiske modelforudsigelser tyder på, at suturstrukturer fundet i en række naturlige manifestationer har udviklet sig til deres optimale geometrier for at opnå den bedste dæmpningsydelse
- Sådan beregnes procentdel reduktion
- Kraftfuldt mikroskop fanger det første billede af nanoscaffold, der fremmer cellebevægelse
- Deep-sea Roombas vil kæmme havbunden til DDT affaldsfade nær Catalina Island
- Alt hvad du behøver at vide om denne uges total måneformørkelse
- SoftBank mobilenhed i rekordhøj børsnotering, men markedsdebut flopper
- Rensevand med smart rust og magneter


