Når træ brændes, hvordan sammenlignes massen af produkter med reaktanter?
Her er hvorfor:
* reaktanter: Træ (for det meste cellulose) og ilt fra luften.
* Produkter: Kuldioxid (CO2), vand (H2O), aske og en lille mængde andre gasser.
Når træforbrændinger, reagerer det med ilt i en proces kaldet forbrænding. De kemiske bindinger i træmolekylerne går i stykker, og der dannes nye bindinger med ilt, hvilket producerer CO2 og H2O. En lille mængde af massen omdannes også til varme og lysenergi. Denne energiudgivelse er grunden til, at træforbrændinger.
Den manglende masse:
Mens masse konserveres, omdannes en lille mængde masse til energi under forbrænding, ifølge Einsteins berømte ligning E =MC². Denne masse masse er så lille, at den praktisk talt ikke kan påvises.
Så den samlede masse af produkterne er lidt mindre end reaktanternes masse, fordi en lille mængde masse omdannes til energi.
 Varme artikler
Varme artikler
-
 Forskere opretter en enhed til at identificere risici for brystkræftDemonstration af koncentrationsgradient i mikrofluidsystem ved hjælp af røde og blå farvestofopløsninger. Kredit:Purdue University Forskere ved Purdue University er ved at skabe en enhed, som de h
Forskere opretter en enhed til at identificere risici for brystkræftDemonstration af koncentrationsgradient i mikrofluidsystem ved hjælp af røde og blå farvestofopløsninger. Kredit:Purdue University Forskere ved Purdue University er ved at skabe en enhed, som de h -
 Søger havet, og bakteriekampe, til nye antibiotikaCameron Currie, ret, med den amerikanske energiminister Steven Chu i Microbial Sciences Building i 2012. Kredit:Jeff Miller Alexander Flemings opdagelse af penicillin - verdens første naturlige an
Søger havet, og bakteriekampe, til nye antibiotikaCameron Currie, ret, med den amerikanske energiminister Steven Chu i Microbial Sciences Building i 2012. Kredit:Jeff Miller Alexander Flemings opdagelse af penicillin - verdens første naturlige an -
 Forskere bringer polymerer i fokus på atomskalaEn gengivelse (grå og pink) af den molekylære struktur af en peptoid polymer, der blev undersøgt af et team ledet af Berkeley Lab og UC Berkeley. Holdets succes med at afbilde polymerers struktur i at
Forskere bringer polymerer i fokus på atomskalaEn gengivelse (grå og pink) af den molekylære struktur af en peptoid polymer, der blev undersøgt af et team ledet af Berkeley Lab og UC Berkeley. Holdets succes med at afbilde polymerers struktur i at -
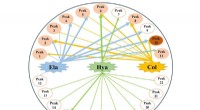 Potentielle anti-aldringskomponenter af Moringa oleifera bladNetværksdiagram over multikomponent- og multi-target-interaktioner af Moringa oleifera-blade. Kredit:WBG Moringa oleifera Lam., også kendt som Miracle Tree, primært afledt fra Indien, er nu vidt ud
Potentielle anti-aldringskomponenter af Moringa oleifera bladNetværksdiagram over multikomponent- og multi-target-interaktioner af Moringa oleifera-blade. Kredit:WBG Moringa oleifera Lam., også kendt som Miracle Tree, primært afledt fra Indien, er nu vidt ud
- Bee-Zed-asteroidens stabile retrograde kredsløb forklares
- Hvad er kulenergi?
- Palcacocha-isfald viser risikosårbarheder i Peru
- Lysbaseret system lægger grundlag for kontinuerlig overvågning af havets plastikpartikler
- Betydningen af en periodisk tabel
- Kemiske tendenser i høj termoelektrisk ydeevne bevist i pyrit-type dicalcogenider


