Er et vandmolekyle polært?
Her er hvorfor:
* form: Vandmolekyler har en bøjet form på grund af de to ensomme par elektroner på iltatomet.
* Elektronegativitet: Oxygen er mere elektronegativ end brint, hvilket betyder, at det tiltrækker elektroner stærkere.
* opladningsfordeling: Oxygenatomet i vand har en delvis negativ ladning (Δ-), mens brintatomerne har delvis positive ladninger (Δ+). Denne ujævne fordeling af ladning skaber et dipolmoment, hvilket gør molekylet polært.
Tænk på det sådan: Vandmolekylet er som en lille magnet med en positiv og negativ ende. Denne polaritet er afgørende for mange af vandets unikke egenskaber, såsom:
* stærk brintbinding: Polære vandmolekyler danner stærke brintbindinger med hinanden, hvilket fører til høj overfladespænding, højt kogepunkt og evnen til at opløse mange polære stoffer.
* Fremragende opløsningsmiddel: Water's polaritet giver det mulighed for at opløse mange ioniske forbindelser og polære molekyler, hvilket gør det til et fremragende opløsningsmiddel for livsprocesser.
 Varme artikler
Varme artikler
-
 Nøglebyggesten til organiske molekyler opdaget i meteoritterEt fragment af Murchison-meteoritten, en af de tre kulstofrige meteoritter, der blev udtaget i denne undersøgelse. Kredit:Daniel P. Glavin Forskere fra Japan og USA har bekræftet tilstedeværelse
Nøglebyggesten til organiske molekyler opdaget i meteoritterEt fragment af Murchison-meteoritten, en af de tre kulstofrige meteoritter, der blev udtaget i denne undersøgelse. Kredit:Daniel P. Glavin Forskere fra Japan og USA har bekræftet tilstedeværelse -
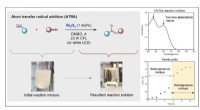 Lysere fremtiden for halvlederbaserede fotokatalytiske processerAtom transfer radikal addition (ATRA) reaktion mellem diethylbrommalonat (DEBM) og 5-hexen-1-ol som en reaktionsmodel. Kredit:Dr. Paola Riente Et samarbejde mellem Pericàs-gruppen med Prof. Timoth
Lysere fremtiden for halvlederbaserede fotokatalytiske processerAtom transfer radikal addition (ATRA) reaktion mellem diethylbrommalonat (DEBM) og 5-hexen-1-ol som en reaktionsmodel. Kredit:Dr. Paola Riente Et samarbejde mellem Pericàs-gruppen med Prof. Timoth -
 Låser op for effektiv lys-energikonvertering med stabile koordinationsnanoarkKredit:Hiroshi Nishihara fra Tokyo University of Science To-dimensionelle nanosheets lavet af bindinger mellem metalatomer og organiske molekyler er attraktive kandidater til fotoelektrisk omdanne
Låser op for effektiv lys-energikonvertering med stabile koordinationsnanoarkKredit:Hiroshi Nishihara fra Tokyo University of Science To-dimensionelle nanosheets lavet af bindinger mellem metalatomer og organiske molekyler er attraktive kandidater til fotoelektrisk omdanne -
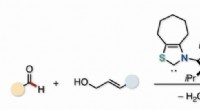 Partnere i katalyse:En effektiv vej til umættede ketonerDen samvirkende virkning af en organokatalysator og en palladiumkatalysator muliggjorde en første dehydrerende direkte allylering mellem aldehyder og allylalkoholer for at producere β, γ-umættede keto
Partnere i katalyse:En effektiv vej til umættede ketonerDen samvirkende virkning af en organokatalysator og en palladiumkatalysator muliggjorde en første dehydrerende direkte allylering mellem aldehyder og allylalkoholer for at producere β, γ-umættede keto
- Hvad hedder den midterste del af en solspot?
- En metode til fremstilling af 3D-Bose-Einstein-kondensater ved hjælp af laserkøling
- Retsmedicinsk videnskab er ikke pålidelig eller upålidelig:Det afhænger af de spørgsmål, du for…
- Forstå modstandsdygtigheden af barriereøer og kystklitter efter storme
- NASA undersøger Dorians nedbør, temperaturer langs Carolinas kyst
- Hvad er en springvand med kogende vand og damp?


