Hvad er volumenet på 84,6 gram helium ved STP?
1. Forstå STP (standardtemperatur og tryk)
* Temperatur: 0 ° C (273,15 K)
* tryk: 1 atm (101.325 kPa)
2. Brug den ideelle gaslov
Den ideelle gaslov vedrører tryk (P), volumen (V), antal mol (N), den ideelle gaskonstant (R) og temperatur (T):
PV =NRT
3. Bestem antallet af mol (n)
* Molær masse af helium (HE): 4,0026 g/mol
* Antal mol (n) =masse (m) / molær masse (m)
* n =84,6 g / 4,0026 g / mol =21,14 mol
4. Vælg den relevante gaskonstant (R)
* r =0,0821 l · atm/mol · k (Denne værdi fungerer, når trykket er i pengeautomat, og volumen er i liter)
5. Løs for volumen (v)
* V =(NRT) / P
* V =(21,14 mol * 0,0821 L · ATM / mol · K * 273,15 K) / 1 atm
* V ≈ 471,7 liter
Derfor er volumenet på 84,6 gram helium ved STP ca. 471,7 liter.
Sidste artikelHvordan finder du ud af, hvad Atom har med kun elektronerne?
Næste artikelHvad er kunstige børster lavet af?
 Varme artikler
Varme artikler
-
 Var ursuppen en solid pre-protein gryderet?De første livspolymerer kan være opstået ved en daglig proces, der stadig observeres på Jorden i dag, såsom gentagen tørring og genopfyldning af damvand. Kredit:Ram Krishnamurthy / Center for Chemical
Var ursuppen en solid pre-protein gryderet?De første livspolymerer kan være opstået ved en daglig proces, der stadig observeres på Jorden i dag, såsom gentagen tørring og genopfyldning af damvand. Kredit:Ram Krishnamurthy / Center for Chemical -
 Forskere forenkler små strukturer konstruktion dryp for drypDer vises tre laboratorieprøver i faldende størrelse. Ringene blev hærdet i en centrifuge ved hjælp af acceleration til at kontrollere længdeskalaen af dråbestrukturer, som kan bruges til at oprette
Forskere forenkler små strukturer konstruktion dryp for drypDer vises tre laboratorieprøver i faldende størrelse. Ringene blev hærdet i en centrifuge ved hjælp af acceleration til at kontrollere længdeskalaen af dråbestrukturer, som kan bruges til at oprette -
 Kemikere udvikler en ny teknologi til at forhindre lithium-ion-batterier i at antændeGasserne byggede sig op og fik det ikke-beskyttede batteri (til venstre) til at svulme op. Det kan føre til en eksplosion. Det beskyttede batteri (til højre) forbliver fladt, da det beskyttende lag bl
Kemikere udvikler en ny teknologi til at forhindre lithium-ion-batterier i at antændeGasserne byggede sig op og fik det ikke-beskyttede batteri (til venstre) til at svulme op. Det kan føre til en eksplosion. Det beskyttede batteri (til højre) forbliver fladt, da det beskyttende lag bl -
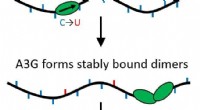 En hvis ved at redigere, to ved vejspærring:Humant protein bekæmper HIV som monomer og dimerForskning for nylig offentliggjort i Naturkommunikation undersøger mulighederne for et humant protein, der hæmmer HIV-1, APOBEC3G (A3G). Papiret fremhæver arbejdet af Northeastern Physics professor
En hvis ved at redigere, to ved vejspærring:Humant protein bekæmper HIV som monomer og dimerForskning for nylig offentliggjort i Naturkommunikation undersøger mulighederne for et humant protein, der hæmmer HIV-1, APOBEC3G (A3G). Papiret fremhæver arbejdet af Northeastern Physics professor
- Kunstig hals kunne en dag hjælpe med at få folk til at tale
- Delfinspil:mere end børneleg?
- Til ros for den store pixel:Gaming har et retro-øjeblik
- 10 nøgler til at integrere sundhed i by- og transportplanlægning
- FN-rapport om havene, frosne zoner:fakta
- Forskere diskuterer MIT og Legacy of Slavery -projektet


