Lås eller låner strontium elektroner?
Her er hvorfor:
* strontiums position på den periodiske tabel: Strontium er i gruppe 2 i den periodiske tabel, også kendt som de alkaliske jordmetaller.
* Elektronkonfiguration: Strontium har to elektroner i sin yderste skal (valenselektroner).
* tendens til at miste elektroner: Elementer i denne gruppe har en stærk tendens til at miste disse to valenselektroner for at opnå en stabil elektronkonfiguration som de ædle gasser.
Derfor danner strontium let en +2 -kation (SR²⁺) ved at miste to elektroner.
 Varme artikler
Varme artikler
-
 Enzymstrukturer belyser mekanismen bag bakteriers bioremedieringsevneBakterie, som mennesker og dyr, skal spise. Sommetider, de forbruger et forurenende stof i miljøet, som mennesker ønsker at slippe af med, en proces kaldet bioremediering. At undersøge de enzymer, der
Enzymstrukturer belyser mekanismen bag bakteriers bioremedieringsevneBakterie, som mennesker og dyr, skal spise. Sommetider, de forbruger et forurenende stof i miljøet, som mennesker ønsker at slippe af med, en proces kaldet bioremediering. At undersøge de enzymer, der -
 Mod 4D-print med strukturelle farverFarven på den blå tarantel (Poecilotheria metallica) kommer fra præcist arrangerede nanokrystaller. Det krystallinske array fungerer som et spejl, der kun reflekterer en bestemt bølgelængde af indkomm
Mod 4D-print med strukturelle farverFarven på den blå tarantel (Poecilotheria metallica) kommer fra præcist arrangerede nanokrystaller. Det krystallinske array fungerer som et spejl, der kun reflekterer en bestemt bølgelængde af indkomm -
 Forskere tilbyder designer store atomer efter behovDisse sekskantede korn af silica, når den suspenderes i en flydende krystal, kan ligne elementer i det periodiske system. Kredit:Smalyukh lab I en ikke så fjern fremtid, forskere kan muligvis bygg
Forskere tilbyder designer store atomer efter behovDisse sekskantede korn af silica, når den suspenderes i en flydende krystal, kan ligne elementer i det periodiske system. Kredit:Smalyukh lab I en ikke så fjern fremtid, forskere kan muligvis bygg -
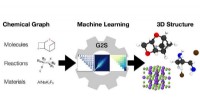 Fra kemiske grafer til strukturerMaskinlæringsmodellen Graph2Structure bruger grafer af kemiske forbindelser (venstre) til at forudsige deres 3D-koordinater (højre). Kredit:Dominik Lemm, Universitetet i Wien 3D-konfigurationer af
Fra kemiske grafer til strukturerMaskinlæringsmodellen Graph2Structure bruger grafer af kemiske forbindelser (venstre) til at forudsige deres 3D-koordinater (højre). Kredit:Dominik Lemm, Universitetet i Wien 3D-konfigurationer af
- Katastrofale doriske pund Bahamas, USA evakuerer kysten
- Nyt bevis afslører grundlæggende grænser for videnskabelig viden
- Forskerteam udvikler ultrahøj følsomhed i nanoskala mikrobølgedetektorer
- Twisted-grafenmodel udviser kompleks elektronisk adfærd
- Hvad er en sang til at huske planeterne ved at udelukke Pluto?
- Brug af militært sprog er måske ikke den bedste tilgang til COVID og folkesundhed


