Hvad er teorien om rust?
rust er en form for korrosion:
* Korrosion er en naturlig proces, der involverer forringelse af et materiale på grund af dets reaktion med dets miljø.
* rust henviser specifikt til korrosion af jern og dets legeringer (som stål).
Den kemiske proces med rustning:
1. Oxidation: Jern reagerer med ilt i nærvær af vand (eller fugt).
2. Elektrokemisk reaktion: Reaktionen er elektrokemisk, hvilket betyder, at der er en overførsel af elektroner mellem jernatomer og iltatomer.
3. Dannelse af jernoxid: Jernen mister elektroner og kombineres med ilt for at danne jernoxid (Fe₂o₃), der almindeligt er kendt som rust.
faktorer, der påvirker rustformation:
* tilstedeværelse af vand: Rusting kræver vand eller fugt. Dette er grunden til, at jern ruster hurtigere i fugtige miljøer.
* tilstedeværelse af ilt: Oxygen er afgørende for, at den kemiske reaktion forekommer.
* elektrolytter: Salt, syrer og andre elektrolytter kan fremskynde rustprocessen ved at fungere som katalysatorer.
* Temperatur: Højere temperaturer kan fremskynde reaktionshastigheden.
* overfladeareal: Et større overfladeareal udsætter mere jern for ilt og vand, hvilket øger hastigheden af rustdannelse.
Forebyggelse af rust:
* Beskyttelsesbelægninger: Maling, olie og andre belægninger skaber en barriere mellem jernet og dets miljø.
* galvanisering: Et lag med zink påføres jern, der fungerer som et offermetal. Zinkkorroder i stedet for jernet.
* legering: Tilføjelse af andre metaller til jern kan skabe mere korrosionsbestandige legeringer.
* Kontroller miljøet: At undgå vand og fugtige forhold kan bremse rustdannelsen.
Kortfattet: Rust er en kompleks kemisk proces, der involverer oxidation af jern i nærvær af ilt og vand. At forstå de faktorer, der påvirker rusten, giver os mulighed for at udvikle metoder til forebyggelse og håndtering af korrosion.
 Varme artikler
Varme artikler
-
 Kemiker viser, at intermolekylære interaktioner kan opnå hidtil ukendte dimensionerKredit:The Journal of Physical Chemistry Letters Intermolekylære interaktioner er de kræfter, der vedrører molekyler. Generelt strækker disse interaktioner sig næppe ud over molekylernes grænser.
Kemiker viser, at intermolekylære interaktioner kan opnå hidtil ukendte dimensionerKredit:The Journal of Physical Chemistry Letters Intermolekylære interaktioner er de kræfter, der vedrører molekyler. Generelt strækker disse interaktioner sig næppe ud over molekylernes grænser. -
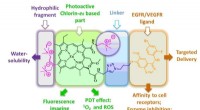 Nye meget selektive antitumor fotodynamiske terapimidler syntetiseretStrukturen af det foreslåede fotosensibilisatorkonjugat. Kredit:Lobachevsky University Et team af forskere fra Lobachevsky University (Nizhny Novgorod, Rusland) ledet af professor Alexei Fedorov
Nye meget selektive antitumor fotodynamiske terapimidler syntetiseretStrukturen af det foreslåede fotosensibilisatorkonjugat. Kredit:Lobachevsky University Et team af forskere fra Lobachevsky University (Nizhny Novgorod, Rusland) ledet af professor Alexei Fedorov -
 En mulig afslutning på evige kemikalierKredit:Marla Bereni/UCR Syntetiske kemikalier kendt som per- og polyfluoralkyler, eller PFAS, indeholder bindinger mellem kulstof- og fluoratomer, der anses for at være de stærkeste i organisk kem
En mulig afslutning på evige kemikalierKredit:Marla Bereni/UCR Syntetiske kemikalier kendt som per- og polyfluoralkyler, eller PFAS, indeholder bindinger mellem kulstof- og fluoratomer, der anses for at være de stærkeste i organisk kem -
 Når man ændrer et atom, bliver molekyler bedreKredit:pexels/CC0 Udvikling og forbedring af lægemidler spiller den centrale rolle i den igangværende kamp mod sygdomme hos mennesker. Organisk syntese er det felt, der muliggør disse udviklinger,
Når man ændrer et atom, bliver molekyler bedreKredit:pexels/CC0 Udvikling og forbedring af lægemidler spiller den centrale rolle i den igangværende kamp mod sygdomme hos mennesker. Organisk syntese er det felt, der muliggør disse udviklinger,
- Snapchat:Sådan lykkedes det forsvindende foto-appen ikke at falme
- 3 Metoder til løsning af systemer af ligninger
- En taksonomisk kategori mellem kongerige og klasse er.?
- Afbrydelse, dæmonisering, befrielse, og normødelæggelse:Donald J. Trumps retoriske signatur
- Hvad er et eksempel på Basin Landform?
- Realkreditkrise:Skyld skylden på banken?


