Hvorfor er Diamond det sværeste stof?
1. Stærke kovalente obligationer:
* Diamond's atomer er arrangeret i en tetrahedral gitter. Hvert carbonatom danner fire stærke kovalente bindinger med dets nærliggende carbonatomer.
* Disse obligationer er ekstremt stærke og kræver en betydelig mængde energi for at bryde. Dette giver diamant sin høje hårdhed og modstand mod ridning.
2. Tæt pakket struktur:
* Det tetrahedrale arrangement af carbonatomer i diamant skaber en tæt pakket, stiv struktur.
* Denne struktur minimerer rummet mellem atomer, hvilket gør det ekstremt vanskeligt at deformere.
3. Højt smeltepunkt:
* De stærke kovalente bindinger i diamant kræver en høj temperatur for at bryde. Dette betyder et meget højt smeltepunkt, hvilket yderligere bidrager til dets hårdhed.
4. Fravær af spaltningsfly:
* I modsætning til mange andre mineraler har Diamond ikke forskellige spaltningsplaner. Spaltningsfly er svage områder, hvor et mineral let kan bryde.
* Fraværet af disse fly i diamant gør det vanskeligt at brud.
Andre faktorer:
* Diamonds hårdhed er også påvirket af faktorer som renhed og krystallinsk struktur. Perfekt ren og godt krystalliserede diamanter er de sværeste.
Vigtig note:
Mens diamant er det sværeste naturligt forekommende stof, er nogle syntetiske materialer, såsom kubisk bornitrid (CBN), endnu sværere. Imidlertid er Diamond stadig den hårdeste naturlige fundne mineral.
 Varme artikler
Varme artikler
-
 Pålideligt simulerende polyurethanskumPU -udvidelsessimulering med FOAM til fremstilling af en køler. Kredit:Fraunhofer ITWM Autostole, madrasser og isoleringsmaterialer er ofte lavet af polyurethanskum. Opskummingsprocessen for de fl
Pålideligt simulerende polyurethanskumPU -udvidelsessimulering med FOAM til fremstilling af en køler. Kredit:Fraunhofer ITWM Autostole, madrasser og isoleringsmaterialer er ofte lavet af polyurethanskum. Opskummingsprocessen for de fl -
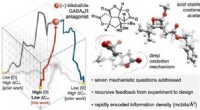 Kemikere udvikler rammer for at muliggøre effektiv syntese af informationstætte molekylerKredit:ACS Et team ledet af forskere ved Scripps Research har udviklet en teoretisk tilgang, der kan lette processen med at gøre meget kompleks, kompakte molekyler. Sådanne molekyler findes ofte
Kemikere udvikler rammer for at muliggøre effektiv syntese af informationstætte molekylerKredit:ACS Et team ledet af forskere ved Scripps Research har udviklet en teoretisk tilgang, der kan lette processen med at gøre meget kompleks, kompakte molekyler. Sådanne molekyler findes ofte -
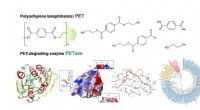 Strukturel indsigt i den molekylære mekanisme ved PET -nedbrydningStrukturel indsigt i den molekylære mekanisme ved poly (ethylenterephthalat) nedbrydning og det fylogenetiske træ af mulige PET -nedbrydende enzymer. Kredit:KAIST Et KAIST metabolisk ingeniørunder
Strukturel indsigt i den molekylære mekanisme ved PET -nedbrydningStrukturel indsigt i den molekylære mekanisme ved poly (ethylenterephthalat) nedbrydning og det fylogenetiske træ af mulige PET -nedbrydende enzymer. Kredit:KAIST Et KAIST metabolisk ingeniørunder -
 Forskere skaber lokkemaling, der lurer infrarøde kameraerBogstaverne C-A-L fremstår seje, selvom miljøet er varmt. UC Berkeley -ingeniører udvikler et lokkedue, der lader infrarøde kameraer til at opfatte en bestemt temperatur frem for objektets faktiske te
Forskere skaber lokkemaling, der lurer infrarøde kameraerBogstaverne C-A-L fremstår seje, selvom miljøet er varmt. UC Berkeley -ingeniører udvikler et lokkedue, der lader infrarøde kameraer til at opfatte en bestemt temperatur frem for objektets faktiske te
- Hvad er formlen for et bariumatom hvert to fluoratomer?
- True crime-underholdning kan kaste lys over kolde sager, men hjælper det eller hindrer det, at retf…
- Debunking The Perpetual Motion Myth:Hvad er nulpunktsenergi?
- 3D-trykte kunstige hornhinder ligner menneskelige
- Hvor mange meter er i 18 meter?
- Teknisk fejl udsætter NASAs satellitopsendelse


