Hvordan er carbonatomerne i et benzenmolekyle arrangeret?
Her er en sammenbrud:
* seks carbonatomer: Kernen i benzenmolekylet består af seks carbonatomer.
* plan struktur: Disse seks carbonatomer ligger i det samme plan og danner en flad, hexagonal form.
* skiftende enkelt- og dobbeltobligationer: Carbonatomerne er forbundet med skiftende enkelt- og dobbeltbindinger. Dette skaber et system med delokaliserede elektroner over og under ringen. Denne delokalisering er en nøglefunktion i Benzens stabilitet og reaktivitet.
Det specielle arrangement af carbonatomerne med de vekslende enkelt- og dobbeltbindinger giver benzen sine unikke egenskaber, herunder:
* Høj stabilitet: De delokaliserede elektroner gør ringen meget stabil og ureaktiv sammenlignet med andre umættede kulbrinter.
* Aromatisk karakter: Dette specielle arrangement af elektroner og bindinger giver benzen sin aromatiske karakter, der påvirker dens kemiske opførsel.
Fortæl mig, hvis du har flere spørgsmål om strukturen eller egenskaberne af benzen!
 Varme artikler
Varme artikler
-
 Førsteklasses YEATS-hæmmere, der viser løfte om leukæmibehandlingDr. Xiang David Li og hans forskningsgruppe ved HKU Institut for Kemi. Kredit:@The University of Hong Kong Et forskerhold ledet af Dr. Xiang David Li fra Institut for Kemi ved University of Hong K
Førsteklasses YEATS-hæmmere, der viser løfte om leukæmibehandlingDr. Xiang David Li og hans forskningsgruppe ved HKU Institut for Kemi. Kredit:@The University of Hong Kong Et forskerhold ledet af Dr. Xiang David Li fra Institut for Kemi ved University of Hong K -
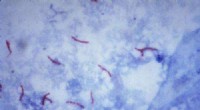 Papirbaseret tuberkulosetest kan øge diagnoser i udviklingslandeDette mikrofotografi afslører Mycobacterium tuberculosis-bakterier ved hjælp af syrefast Ziehl-Neelsen-farve; Forstørret 1000 X. De syrefaste pletter afhænger af mykobakteriers evne til at tilbagehold
Papirbaseret tuberkulosetest kan øge diagnoser i udviklingslandeDette mikrofotografi afslører Mycobacterium tuberculosis-bakterier ved hjælp af syrefast Ziehl-Neelsen-farve; Forstørret 1000 X. De syrefaste pletter afhænger af mykobakteriers evne til at tilbagehold -
 Unik kemi - som en dag kan hjælpe med at bekæmpe alvorlig sygdom - fundet i den newzealandske glø…Dr Miriam Sharpe, Institut for Biokemi. Kredit:University of Otago University of Otago forskere i New Zealand har hjulpet med at afdække, hvordan newzealandske glødorme producerer deres glød. En f
Unik kemi - som en dag kan hjælpe med at bekæmpe alvorlig sygdom - fundet i den newzealandske glø…Dr Miriam Sharpe, Institut for Biokemi. Kredit:University of Otago University of Otago forskere i New Zealand har hjulpet med at afdække, hvordan newzealandske glødorme producerer deres glød. En f -
 Forskere bruger neurale netværk til lugtgenkendelseKredit:National Research University Higher School of Economics Forskere fra HSE Laboratory of Space Research, Teknologier, Systemer og processer har anvendt hurtigt lærende kunstige intelligenssys
Forskere bruger neurale netværk til lugtgenkendelseKredit:National Research University Higher School of Economics Forskere fra HSE Laboratory of Space Research, Teknologier, Systemer og processer har anvendt hurtigt lærende kunstige intelligenssys
- Ny, forenklet teknik gør let metallisk nanoskum
- En dæmning lige over Vesterhavet
- Reduktion af miljøpåvirkningen af global sundhedshjælp er afgørende, siger ekspert
- Hvordan levende materialer fra alger bedst kan opfange kulstof
- Bro over koblede farvande:Forskere 3-D-printer laboratorium med fuld væske på en chip
- Hvad er isolatorer?


