I en kemisk reaktion kombineres 300 gram reaktant A med 100 b. både og til færdiggørelse. Hvor meget vejer produktet?
* bevarelse af masse: I en kemisk reaktion skal reaktanternes samlede masse svarer til den samlede masse af produkterne. Dette er kendt som loven om bevarelse af masse.
* ukendt støkiometri: Vi kender ikke den kemiske formel for reaktant A eller B eller den afbalancerede kemiske ligning for reaktionen. Dette betyder, at vi ikke kan bestemme det forhold, hvor de reagerer, eller produktets molekylvægt.
Eksempel:
Lad os sige, at reaktionen er:
A + 2B → AB₂
* Hvis A har en molekylvægt på 100 g/mol og B har en molekylvægt på 50 g/mol, ville produktet AB₂ have en molekylvægt på 200 g/mol.
* I dette tilfælde ville reaktionen forbruge alle B og efterlade nogle ureagerede. Produktet vejer 200 gram.
For at løse dette problem har du brug for:
1. de kemiske formler af reaktanter A og B
2. den afbalancerede kemiske ligning for reaktionen
Når du har disse oplysninger, kan du beregne produktets vægt.
Sidste artikelHvad er forskellene mellem metaller og ikke -metaller?
Næste artikelFormidles dug på en fysisk eller kemisk ændring af blad?
 Varme artikler
Varme artikler
-
 Effekter af tværbinderlængde på anionbyttermembranbrændselscellerFremskridt inden for brændselscelleteknologi vil hjælpe os kraftigt med at reducere vores brug af fossile brændstoffer til at generere elektricitet, fører til mindre luftforurening. Kredit:Chris LeBou
Effekter af tværbinderlængde på anionbyttermembranbrændselscellerFremskridt inden for brændselscelleteknologi vil hjælpe os kraftigt med at reducere vores brug af fossile brændstoffer til at generere elektricitet, fører til mindre luftforurening. Kredit:Chris LeBou -
 Metalindustrien er ved at gennemgå en af de største omvæltninger i historien, siger ekspertPotentielt bæredygtig:i dag, elektricitet bruges allerede til elektrolytisk udvinding af aluminium fra dets malme. I dag, elektricitet kommer ofte fra vandkraftværker, men også fra konventionelle kraf
Metalindustrien er ved at gennemgå en af de største omvæltninger i historien, siger ekspertPotentielt bæredygtig:i dag, elektricitet bruges allerede til elektrolytisk udvinding af aluminium fra dets malme. I dag, elektricitet kommer ofte fra vandkraftværker, men også fra konventionelle kraf -
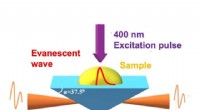 Terahertz-bølger afslører skjulte processer i ultrahurtig kunstig fotosynteseOpsætning til tidsopløst terahertz-dæmpet totalreflektion (TR-ATR) spektroskopi. Kredit:Osaka University Et team af forskere fra Osaka University, i samarbejde med Tokyo Institute of Technology, d
Terahertz-bølger afslører skjulte processer i ultrahurtig kunstig fotosynteseOpsætning til tidsopløst terahertz-dæmpet totalreflektion (TR-ATR) spektroskopi. Kredit:Osaka University Et team af forskere fra Osaka University, i samarbejde med Tokyo Institute of Technology, d -
 Forskere skubber mikroskopi til sub-molekylær opløsningAt være i stand til at se den indre funktion af de grundlæggende enheder i alt stof er virkelig fantastisk, og det er et af hovedmålene, vi har forfulgt hos CaSTL i mere end et årti, ” siger studie me
Forskere skubber mikroskopi til sub-molekylær opløsningAt være i stand til at se den indre funktion af de grundlæggende enheder i alt stof er virkelig fantastisk, og det er et af hovedmålene, vi har forfulgt hos CaSTL i mere end et årti, ” siger studie me
- Forskere afslører, hvordan salt kan spille ind i klimaopvarmningen
- Hvordan kan jeg kontrollere den aktuelle månefase?
- Hvordan ved arkæologer, hvor de skal grave?
- Forskere bruger ny tilgang til at skabe triangulenmolekyle
- Sociale netværk på bagkant, når digitale kampagner udvider taktikken
- Ny bog viser, hvordan oldgræsk skrift hjælper os med at forstå nutidens miljøkriser


