Den kenetiske teori om stof siger, at atomer og molekyler er?
* i konstant, tilfældig bevægelse. Denne bevægelse er ikke ensartet eller forudsigelig, men temmelig kaotisk og ændrer konstant.
* besidder kinetisk energi. Denne energi er direkte relateret til deres temperatur. Jo højere temperatur, jo hurtigere bevæger partiklerne sig, og jo mere kinetisk energi besidder de.
* interagerer med hinanden gennem kollisioner. Disse kollisioner kan være elastisk (energi konserveres) eller uelastisk (energi går tabt), og de påvirker stoffets samlede opførsel.
* den gennemsnitlige kinetiske energi for partiklerne er proportional med den absolutte temperatur. Dette betyder, at når temperaturen øges, øges partiklernes gennemsnitlige hastighed også.
Disse egenskaber forklarer de forskellige tilstande af stof (faste, flydende, gas) og ændringerne mellem dem. I et fast stof er partiklerne for eksempel tæt pakket og vibrerer på plads, mens de i en gas er langt fra hinanden og bevæger sig frit.
Sidste artikelEr et atom et biotisk eller abiotisk?
Næste artikelHvad sker der med et atom, når det mister et elektron?
 Varme artikler
Varme artikler
-
 Forbedring af ydeevnen af metal-organiske rammematerialerMikrograffoto (samlet bredde ca. 1, 5 mm), der viser det nye adsorberende materiale, der blev fremstillet ved anvendelse af et poppelblad som skabelon. Kanalarkitekturen er tydeligt mærkbar. Tegninger
Forbedring af ydeevnen af metal-organiske rammematerialerMikrograffoto (samlet bredde ca. 1, 5 mm), der viser det nye adsorberende materiale, der blev fremstillet ved anvendelse af et poppelblad som skabelon. Kanalarkitekturen er tydeligt mærkbar. Tegninger -
 Forskere simulerer processen med klæbende slidComputersimuleringen viser klæbende slid på en selv-affin overflade. Kredit:LSMS / EPFL Overfladeslid beskriver processen med materialetab, når to overflader kommer i kontakt med hinanden. Det har
Forskere simulerer processen med klæbende slidComputersimuleringen viser klæbende slid på en selv-affin overflade. Kredit:LSMS / EPFL Overfladeslid beskriver processen med materialetab, når to overflader kommer i kontakt med hinanden. Det har -
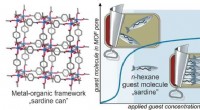 Gæstejustering og defektdannelse under porefyldning i metal-organiske rammefilmDen metalorganiske ramme danner et stillads med nanometerstore porer, som holder molekyler (til venstre). Så længe n-hexangas-molekyler tilsættes til porerne under tryk, justeres molekylerne i en sard
Gæstejustering og defektdannelse under porefyldning i metal-organiske rammefilmDen metalorganiske ramme danner et stillads med nanometerstore porer, som holder molekyler (til venstre). Så længe n-hexangas-molekyler tilsættes til porerne under tryk, justeres molekylerne i en sard -
 Forskerhold skruer op for varmen på 3D-printblækEn 3D-printet blomst demonstrerer kvaliteterne af en multifunktionel printgel, der reagerer på fugt. Kredit:Ke Functional Research Group i Dartmouth. En proces, der bruger varme til at ændre arran
Forskerhold skruer op for varmen på 3D-printblækEn 3D-printet blomst demonstrerer kvaliteterne af en multifunktionel printgel, der reagerer på fugt. Kredit:Ke Functional Research Group i Dartmouth. En proces, der bruger varme til at ændre arran
- Hvad er komponenterne i et ilttilførselssystem?
- Twitter suspenderede 58 millioner konti i 4Q (opdatering)
- Chancen for at finde unge jordlignende planeter højere end tidligere antaget
- Grafenvækst på sølv
- Sådan identificeres vilde svampe i Tennessee
- FTC idømmer Facebook en bøde på 5 mia. tilføjer begrænset tilsyn med privatlivets fred


