Hvorfor har H2O et højere punkt end CO2?
Hydrogenbinding vs. svage intermolekylære kræfter:
* vand (H₂O): Vandmolekyler danner stærke brintbindinger med hinanden. Hydrogenbindinger er en type intermolekylær kraft, hvor et hydrogenatom tiltrækkes af et meget elektronegativt atom som ilt. Disse obligationer er relativt stærke, hvilket kræver en masse energi til at bryde.
* kuldioxid (co₂): Kuldioxidmolekyler er ikke -polære og interagerer primært gennem svage London -spredningskræfter. Disse kræfter er meget svagere end brintbindinger.
kogepunkt og intermolekylære kræfter:
* kogepunkt: Kogepunktet for et stof er den temperatur, hvormed dets damptryk er lig med det omgivende atmosfæriske tryk.
* Intermolekylær kraftstyrke: Jo stærkere de intermolekylære kræfter mellem molekyler, jo mere energi (og derfor højere temperatur) er påkrævet for at bryde dem fra hinanden og lade stoffet overgang til en gas (kog).
Kortfattet:
Vands stærke brintbindinger kræver signifikant mere energi til at overvinde end de svage intermolekylære kræfter i kuldioxid. Dette fører til et meget højere kogepunkt for vand (100 ° C) sammenlignet med kuldioxid (-78,5 ° C).
Sidste artikelHvilket af følgende er ikke en forbindelse - sukker eller guld?
Næste artikelHvad er kulstofindholdet i parafin?
 Varme artikler
Varme artikler
-
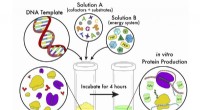 Forenklet metode gør cellefri proteinsyntese mere fleksibel og tilgængeligEn tegneserie af cellefri proteinsyntese, en bioteknologi, der udnytter cellens genetiske kode i et reagensglas. Skematikken repræsenterer en forenklet tilgang, der gør det muligt for forskere at udfø
Forenklet metode gør cellefri proteinsyntese mere fleksibel og tilgængeligEn tegneserie af cellefri proteinsyntese, en bioteknologi, der udnytter cellens genetiske kode i et reagensglas. Skematikken repræsenterer en forenklet tilgang, der gør det muligt for forskere at udfø -
 Forskere opdager ny arkitektur i majsLSU Institut for Kemi Adjunkt Tuo Wang og kolleger er de første til at undersøge en intakt majsplantestilk på atomniveau ved hjælp af højopløsningsteknikker. Kredit:Peggy Greb, USDA Ny forskning i
Forskere opdager ny arkitektur i majsLSU Institut for Kemi Adjunkt Tuo Wang og kolleger er de første til at undersøge en intakt majsplantestilk på atomniveau ved hjælp af højopløsningsteknikker. Kredit:Peggy Greb, USDA Ny forskning i -
 Skylning af tendenser i stofbrug tidligt i COVID-19-pandemienKredit:Pixabay/CC0 Public Domain Ved starten af COVID-19-pandemien, hjemmeboende ordrer og andre restriktioner påvirkede drastisk, hvordan folk boede og arbejdede, resulterer i social isolation
Skylning af tendenser i stofbrug tidligt i COVID-19-pandemienKredit:Pixabay/CC0 Public Domain Ved starten af COVID-19-pandemien, hjemmeboende ordrer og andre restriktioner påvirkede drastisk, hvordan folk boede og arbejdede, resulterer i social isolation -
 Hvor bliver surt øl så... surtØlprøver (til højre) blev indsamlet hver 2.-3. uge for at spore skiftende koncentrationer af organiske syrer og sporkomponenter under lagring i tønder (venstre). Kredit:Bryan Doty/Sour Cellars sur
Hvor bliver surt øl så... surtØlprøver (til højre) blev indsamlet hver 2.-3. uge for at spore skiftende koncentrationer af organiske syrer og sporkomponenter under lagring i tønder (venstre). Kredit:Bryan Doty/Sour Cellars sur
- Talek:Et privat beskedsystem, der skjuler beskedindhold og brugerkommunikationsmønstre
- Er ren luft et rent stof eller en blanding?
- Tests viser lys fremtid for gadonanorør i stamcellesporing
- Ny undersøgelse viser måder at maksimere temperatursænkende fordele ved Chicagos grønne tage
- Ny forskning afslører, hvordan man afslører løgnere ved at distrahere
- Liste over sjove fakta om vandcyklussen


