Hvilke af disse stoffer har det laveste kogepunkt KCL CO2CH2O?
* KCL (kaliumchlorid): Dette er en ionisk forbindelse. Ioniske forbindelser har meget stærke elektrostatiske attraktioner mellem deres ioner, hvilket fører til høje smelte- og kogepunkter.
* CO2 (kuldioxid): Dette er et ikke -polært molekyle. Ikke -polære molekyler har svage London -spredningskræfter, som er de eneste intermolekylære kræfter, der er til stede. Dette resulterer i relativt lave kogepunkter.
* ch2o (formaldehyd): Dette er et polært molekyle. Polære molekyler har dipol-dipol-interaktioner ud over London-spredningskræfter. Dipole-dipol-interaktioner er stærkere end London-spredningskræfter, men stadig svagere end ioniske bindinger.
Derfor vil CO2 (kuldioxid) have det laveste kogepunkt.
Her er hvorfor:
* svageste intermolekylære kræfter: CO2 har kun svage London -spredningskræfter mellem dens molekyler.
* mindre molekylstørrelse: CO2 er et lille molekyle, der yderligere reducerer styrken af disse kræfter.
 Varme artikler
Varme artikler
-
 Ensomme vandmolekyler viser sig at være direktører for supramolekylær kemiBert Meijer, professor i organisk kemi, og postdoktorforsker Nathan van Zee. Kredit:Bart van Overbeeke Forskere inden for supramolekylær kemi støder ofte på overraskende resultater. En brudt forse
Ensomme vandmolekyler viser sig at være direktører for supramolekylær kemiBert Meijer, professor i organisk kemi, og postdoktorforsker Nathan van Zee. Kredit:Bart van Overbeeke Forskere inden for supramolekylær kemi støder ofte på overraskende resultater. En brudt forse -
 Forskere ser revnedannelse i 3-D-printet wolfram i realtidVed at kombinere simuleringer med højhastighedsvideoer taget under laserpulver-bed-fusionsprocessen, LLNL-forskere var i stand til at visualisere overgangen fra duktilt til skørt i 3D-printet wolfram
Forskere ser revnedannelse i 3-D-printet wolfram i realtidVed at kombinere simuleringer med højhastighedsvideoer taget under laserpulver-bed-fusionsprocessen, LLNL-forskere var i stand til at visualisere overgangen fra duktilt til skørt i 3D-printet wolfram -
 Et spil pool i den levende celleIllustration af den nye kemo-optogenetiske metode præsenteret af forskergruppen af Yaowen Wu Kredit:Yaowen Wu, Umeå Universitet Celler skal reagere på miljøændringer og opretholde et afbalancere
Et spil pool i den levende celleIllustration af den nye kemo-optogenetiske metode præsenteret af forskergruppen af Yaowen Wu Kredit:Yaowen Wu, Umeå Universitet Celler skal reagere på miljøændringer og opretholde et afbalancere -
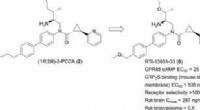 Narkotika gør rotter mindre tilbøjelige til at indtage alkoholKredit:American Chemical Society Alkoholforstyrrelser kan have ødelæggende virkninger på en persons helbred, relationer og økonomi. Men for nogle, den følelse, de får, når de tager en drink, opvej
Narkotika gør rotter mindre tilbøjelige til at indtage alkoholKredit:American Chemical Society Alkoholforstyrrelser kan have ødelæggende virkninger på en persons helbred, relationer og økonomi. Men for nogle, den følelse, de får, når de tager en drink, opvej
- Ny undersøgelse tager en anden tilgang til at vise menneskelig aktivitet, der forårsager jordskæl…
- Udviser byfisk nedsat søvn?
- Er kulhydrater biologiske makromolekyler, der hovedsageligt er sammensat af brint og kulstof?
- Formål med kalkvand med marmorchip?
- Sådan måles glukoseniveauet i Leaves
- Hvad er meningen med en proces, der begynder at overføre materialer og energi i hele skovøkosystem…


