Hvorfor udfører HCL -gas ikke elektricitet, når de opløstes i toluen?
Her er hvorfor:
* Polaritet: HCI er et polært molekyle på grund af forskellen i elektronegativitet mellem brint og klor. Dette skaber en delvis positiv ladning på hydrogenatomet og en delvis negativ ladning på kloratomet.
* Ikke-polære opløsningsmidler: Toluen, et carbonhydrid, er et ikke-polært opløsningsmiddel. Ikke-polære opløsningsmidler er ikke i stand til effektivt at adskille de positive og negative ladninger af polære molekyler som HCI.
* ionisering: For en løsning til at udføre elektricitet har den brug for ioner (ladede partikler) for at transportere den elektriske strøm. I ikke-polære opløsningsmidler som toluen forbliver HCL-molekyler intakte og adskiller sig ikke i ioner (H+ og Cl-).
* Ingen frie ioner: Uden frie ioner i opløsningen er der ingen vej til elektrisk strøm til at strømme, hvilket forklarer den manglende ledningsevne.
I modsætning: Når HCl-gas opløses i vand (et polært opløsningsmiddel), adskiller den sig let i H+ og klodser, hvilket fører til en meget ledende opløsning.
Sidste artikelHvorfor er helium lettere end nitrogen?
Næste artikelKondensationkerner er involveret i dannelsen?
 Varme artikler
Varme artikler
-
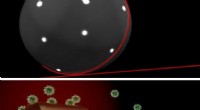 At sætte fokus på livets maskineriEn sensor på en sensor:Laserlys (rødt) skinner (øverst) ind i en mikroperle af glas, som en guld nanorod er fastgjort til. Laserlyset løber rundt om indersiden af mikroperlen og er koncentreret om g
At sætte fokus på livets maskineriEn sensor på en sensor:Laserlys (rødt) skinner (øverst) ind i en mikroperle af glas, som en guld nanorod er fastgjort til. Laserlyset løber rundt om indersiden af mikroperlen og er koncentreret om g -
 Forskere fremstiller gennemsigtig keramik af høj kvalitetKredit:CC0 Public Domain Mid-infrarøde lasere er blevet meget brugt til billeddannelse, opdagelse, diagnostik, miljøovervågning, medicin, industri, forsvar og andre. Til mellem-infrarøde lasersyst
Forskere fremstiller gennemsigtig keramik af høj kvalitetKredit:CC0 Public Domain Mid-infrarøde lasere er blevet meget brugt til billeddannelse, opdagelse, diagnostik, miljøovervågning, medicin, industri, forsvar og andre. Til mellem-infrarøde lasersyst -
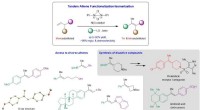 Stereoselektiv alkensyntese med ikke-ædel nikkelkatalyseSkematisk, der viser udviklingen af et nyt Ni-katalyseret system, der konverterer billige og let tilgængelige monosubstituerede olefiner til højværdi tri- og tetrasubstituerede analoger, og dets anv
Stereoselektiv alkensyntese med ikke-ædel nikkelkatalyseSkematisk, der viser udviklingen af et nyt Ni-katalyseret system, der konverterer billige og let tilgængelige monosubstituerede olefiner til højværdi tri- og tetrasubstituerede analoger, og dets anv -
 Biokemikere opdager mekanisme, der hjælper influenzavirus med at udvikle sigVirion vandrere med varierende fitness, illustreret her som beredskab, forsøg på at klatre Folded Peak Mens nogle virioner er for uegnede til at ramme sporet (rød), nogle er tilstrækkeligt egnede til
Biokemikere opdager mekanisme, der hjælper influenzavirus med at udvikle sigVirion vandrere med varierende fitness, illustreret her som beredskab, forsøg på at klatre Folded Peak Mens nogle virioner er for uegnede til at ramme sporet (rød), nogle er tilstrækkeligt egnede til
- Hvordan man opbygger en model af solsystemet ud af balloner
- Vender du tilbage til arbejdspladsen? Sådan holder du fokus på et støjende kontor
- Nyt uhyggeligt, crawly søge- og redningsrobot udviklet
- Den kaotiske tidlige fase af solsystemet
- Er en sonisk boom kontinuerlig, så længe flyet overstiger lydhastigheden?
- Billede:Asteroidernes dans


