Er CF en polær eller ikke -binding?
* Elektronegativitet: Fluor (F) er det mest elektronegative element på den periodiske tabel. Carbon (C) er mindre elektronegativ. Dette betyder, at fluor har en stærkere attraktion for elektroner end kulstof.
* ulig deling: I en CF -binding tilbringer de delte elektroner mere tid tættere på fluoratomet end carbonatomet. Dette skaber en delvis negativ ladning (Δ-) på fluor og en delvis positiv ladning (Δ+) på kulstoffet.
* dipolmoment: Adskillelsen af ladning resulterer i et dipolmoment, hvor den ene ende af bindingen er lidt negativ, og den anden ende er lidt positiv.
Kortfattet: Den signifikante forskel i elektronegativitet mellem kulstof og fluor fører til en ujævn deling af elektroner, hvilket gør CF -bindingspolaren.
 Varme artikler
Varme artikler
-
 Skinnende røntgenlys på perovskiter for bedre solcellerKredit:CC0 Public Domain Opkaldt efter et mineral opdaget i Uralbjergene i Rusland, perovskites har taget i centrum som en klasse af materialer med egenskaber, der kan anvendes på fremtidige elekt
Skinnende røntgenlys på perovskiter for bedre solcellerKredit:CC0 Public Domain Opkaldt efter et mineral opdaget i Uralbjergene i Rusland, perovskites har taget i centrum som en klasse af materialer med egenskaber, der kan anvendes på fremtidige elekt -
 Forskere udvikler metode til at beregne transparente materialers porøsitetForskere fra Far Eastern Federal University (FEFU) har brugt en unik matematisk model til at beregne dataene for 3D-billeder af defekter i mængden af gennemsigtige funktionelle materialer. Det indle
Forskere udvikler metode til at beregne transparente materialers porøsitetForskere fra Far Eastern Federal University (FEFU) har brugt en unik matematisk model til at beregne dataene for 3D-billeder af defekter i mængden af gennemsigtige funktionelle materialer. Det indle -
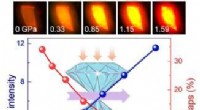 Tryk undertrykker bærerindfangning i 2-D halogenidperovskitFluorescensmikrografer under kompression og PL-intensiteten og bidraget fra de fangede staters emission som funktion af tryk. Kredit:Center for High Pressure Science &Technology Advanced Research
Tryk undertrykker bærerindfangning i 2-D halogenidperovskitFluorescensmikrografer under kompression og PL-intensiteten og bidraget fra de fangede staters emission som funktion af tryk. Kredit:Center for High Pressure Science &Technology Advanced Research -
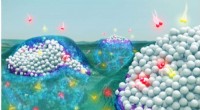 Mystisk organisk skum øger effektiviteten af kemiske reaktioner, kan reducere kemisk affaldIllinois-forskere er en del af et multiinstitutionelt team, der fandt ud af, at opløsningsmidler spontant reagerer med metal-nanopartikler for at danne reaktive komplekser, der kan forbedre katalysato
Mystisk organisk skum øger effektiviteten af kemiske reaktioner, kan reducere kemisk affaldIllinois-forskere er en del af et multiinstitutionelt team, der fandt ud af, at opløsningsmidler spontant reagerer med metal-nanopartikler for at danne reaktive komplekser, der kan forbedre katalysato
- Har vandet, der er opbevaret bag en dæmning, kinetisk energi, før den frigives?
- Hvis du køber et pinligt produkt online, rødmer du så stadig? Ny undersøgelse siger ja
- Hvilken berømt overtro er relateret til kometer?
- Visualisering af global repræsentation for oprindelige nationer
- Hvorfor forekommer en fissionsreaktion lettere end fusionsreaktion?
- Kulfiber kan lagre energi i et køretøjs karosseri


