Tris -puffer som pH ved HCI Hvorfor ikke for natriumacetat?
1. Tris -buffer og HCL
* tris (Tris (hydroxymethyl) aminomethan) er en svag base med en PKA på 8,1.
* hcl er en stærk syre.
* hvordan det fungerer: Når HCL føjes til Tris, reagerer det med Tris-basen for at danne Tris-konjugatsyre (Tris-H+). Dette skaber en pufferopløsning med en pH nær PKA af Tris (ca. 8,1).
2. Natriumacetatbuffer og HCL
* natriumacetat er et salt af en svag syre (eddikesyre) og en stærk base (natriumhydroxid).
* hcl er en stærk syre.
* Hvorfor er det ikke ideelt: Tilsætning af HCI til en natriumacetatbufferopløsning ville forstyrre ligevægten. HCI ville reagere med acetationerne (CH3COO-) til dannelse af eddikesyre (CH3COOH). Dette ville skifte ligevægt mod den sure side, hvilket potentielt kan føre til et signifikant fald i pH og potentielt overskride bufferkapaciteten for acetatbufferen.
Nøgleforskelle:
* Tris -buffer er designet til at arbejde med stærke syrer: Dens svage base -natur giver den mulighed for at acceptere protoner (H+) fra stærke syrer som HCI, hvilket skaber et puffersystem, der modstår pH -ændringer.
* natriumacetatbuffer er mere følsom over for stærke syrer: Fordi det er et salt af en svag syre, kan tilsætning af en stærk syre som HCI hurtigt forbruge acetationerne og forstyrre puffer -ligevægten.
Kortfattet:
Mens både Tris og natriumacetat er nyttige til at skabe pufferopløsninger, ligger deres styrker i forskellige områder. Tris -buffere fungerer godt med stærke syrer, hvilket gør dem egnede til pH -justeringer ved hjælp af HCI. Natriumacetatbuffere er bedre egnet til pH -kontrol i situationer, hvor du har brug for at modstå ændringer på grund af tilsætning af svage syrer eller baser.
 Varme artikler
Varme artikler
-
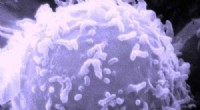 Patientkræftceller vokser pålideligt på nyt 3D-stillads, viser løfte om præcisionsmedicinElektronmikroskopisk billede af en enkelt human lymfocyt. Kredit:Dr. Triche National Cancer Institute En ny 3D-struktur til voksende cellekulturer kan gøre det muligt for læger at teste medicin på
Patientkræftceller vokser pålideligt på nyt 3D-stillads, viser løfte om præcisionsmedicinElektronmikroskopisk billede af en enkelt human lymfocyt. Kredit:Dr. Triche National Cancer Institute En ny 3D-struktur til voksende cellekulturer kan gøre det muligt for læger at teste medicin på -
 At lave tøj af mælkKredit:Piotr Łohunko I EU, beboere spilder anslået 88 millioner tons mad hvert år, ifølge de seneste skøn. Det er omkring 170 kg pr. person. Men hvad nu hvis videnskabsmænd kunne omdanne noget af
At lave tøj af mælkKredit:Piotr Łohunko I EU, beboere spilder anslået 88 millioner tons mad hvert år, ifølge de seneste skøn. Det er omkring 170 kg pr. person. Men hvad nu hvis videnskabsmænd kunne omdanne noget af -
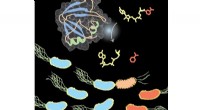 Ny indsigt i plantemikrobiomets molekylære våbenBilledet viser Tne2, et NAD-nedbrydende enzym udskilt gennem type 6 sekretionssystem af den plantebeskyttende bakterie Pseudomonas protegens. Kredit:John Whitney, McMaster University Som alle orga
Ny indsigt i plantemikrobiomets molekylære våbenBilledet viser Tne2, et NAD-nedbrydende enzym udskilt gennem type 6 sekretionssystem af den plantebeskyttende bakterie Pseudomonas protegens. Kredit:John Whitney, McMaster University Som alle orga -
 Kræftceller kan kommunikere over længere afstande i kroppenKredit:Ecole Polytechnique Federale de Lausanne EPFL-forskere har opdaget, at kræftceller bruger exosomer til at kommunikere med hinanden og sende information gennem blodbanen. Dette gennembrud åb
Kræftceller kan kommunikere over længere afstande i kroppenKredit:Ecole Polytechnique Federale de Lausanne EPFL-forskere har opdaget, at kræftceller bruger exosomer til at kommunikere med hinanden og sende information gennem blodbanen. Dette gennembrud åb
- Opgraderet GMRT måler massen af brint i fjerne galakser
- Hvorfor et par dråber vand får whisky til at smage bedre
- Overanstrengt og isoleret:den stigende epidemi af ensomhed i den akademiske verden
- NOx-gasser i dieselbiler:Hvorfor er de så farlige?
- Hvad er den tredje spids i en polariseret beholder, der bruges til?


