Hvis en blanding af to gasser har samlet tryk 5,7 atm. Den ene gas delvis 4,1 atm Hvad er den anden gas?
Daltons lov om delvis pres
Daltons lov siger, at det samlede tryk af en blanding af gasser er lig med summen af de delvise tryk på de individuelle gasser.
Formel:
P total =P 1 + P 2 + ... + p n
Hvor:
* P total er det samlede tryk på blandingen
* P 1 , P 2 , ... p n er det delvise tryk på hver enkelt gas
Beregning:
1. Identificer de kendte værdier:
* P total =5,7 atm
* P 1 =4,1 atm (delvis tryk på en gas)
2. lad p 2 repræsenterer det delvise tryk på den anden gas.
3. Anvend Daltons lov:
5.7 atm =4,1 atm + p 2
4. Løs for p 2 :
P 2 =5,7 atm - 4,1 atm =1,6 atm
Svar: Det delvise tryk på den anden gas er 1,6 atm.
Sidste artikelKan mængden af gas påvirke trykgassen?
Næste artikelHvilken farve skal flammen være på en gaskedel?
 Varme artikler
Varme artikler
-
 Soltårnet udsætter materialer for intens varme for at teste termisk responsKredit:Sandia National Laboratories Sandia National Laboratories bruger sit soltårn til at hjælpe med at vurdere virkningen af ekstreme temperaturændringer på materialer. Testene, nu på deres a
Soltårnet udsætter materialer for intens varme for at teste termisk responsKredit:Sandia National Laboratories Sandia National Laboratories bruger sit soltårn til at hjælpe med at vurdere virkningen af ekstreme temperaturændringer på materialer. Testene, nu på deres a -
 Hvordan edderkoppesilke en dag kunne bruges i kræftbehandlingKredit:Vadym Lesyk/Shutterstock Kræft er samtidig en af de mest almindelige og ødelæggende sygdomme i vores samfund. Så at finde nye måder at behandle det på er en vedvarende videnskabelig udford
Hvordan edderkoppesilke en dag kunne bruges i kræftbehandlingKredit:Vadym Lesyk/Shutterstock Kræft er samtidig en af de mest almindelige og ødelæggende sygdomme i vores samfund. Så at finde nye måder at behandle det på er en vedvarende videnskabelig udford -
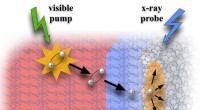 Langsom ladningsgenerering spiller en stor rolle i modelmateriale til solcellerSynlig pumpe / røntgensonde fotoelektronspektroskopi overvåger exciton-migrering og ladningsgenerering i en molekylær heterojunction mellem en kobber-phthalocyanin (CuPc) donor og en fulleren-baseret
Langsom ladningsgenerering spiller en stor rolle i modelmateriale til solcellerSynlig pumpe / røntgensonde fotoelektronspektroskopi overvåger exciton-migrering og ladningsgenerering i en molekylær heterojunction mellem en kobber-phthalocyanin (CuPc) donor og en fulleren-baseret -
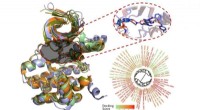 Computermodellering af WNK-kinasehæmmere kunne tilbyde nye værktøjer til at forstå hypertensionKredit:North Carolina State University Forskere fra North Carolina State University har modelleret og analyseret bindingsmåderne for 210 molekyler, der tidligere er rapporteret at hæmme funktionen
Computermodellering af WNK-kinasehæmmere kunne tilbyde nye værktøjer til at forstå hypertensionKredit:North Carolina State University Forskere fra North Carolina State University har modelleret og analyseret bindingsmåderne for 210 molekyler, der tidligere er rapporteret at hæmme funktionen
- Hvorfor smelter polære regioner?
- Ny undersøgelse viser fordelene ved undervurderet saltmarsk
- Forskere foreslår en strategi til at evaluere fototermisk tumorterapi i realtid
- Den kriseramte Nissan CEO trækker sig efter en lønundersøgelse
- Bike to Work Week:Er e-cykler svaret på sundheds-, trafik- og miljøproblemer?
- Mikro-miljømæssige påvirkninger på kunstige mikromotorer


