Hvilke typer intermolekylære kræfter kan der eksistere mellem molekyler jod?
Her er hvorfor:
* jod er ikke -polær: I₂ -molekylet er symmetrisk med elektronerne jævnt fordelt. Dette betyder, at det ikke har noget permanent dipolmoment.
* ldfs opstår fra midlertidige dipoler: Selvom jod er ikke -polær, er dens elektroner konstant i bevægelse. På ethvert givet øjeblik kan der være en midlertidig ubalance i elektronfordelingen, hvilket skaber en midlertidig, øjeblikkelig dipol. Denne midlertidige dipol kan derefter inducere en midlertidig dipol i et nærliggende jodmolekyle. Disse svage, midlertidige attraktioner er LDF'er.
Mens jod også kan opleve dipolinducerede dipolkræfter, er disse markant svagere end LDF'er på grund af manglen på permanente dipoler.
Sammenfattende er den dominerende intermolekylære kraft i jod i London Dispersion Forces (LDFS).
Sidste artikelHvad er elektronkonfiguration af B3?
Næste artikelHvad skal kemiske reaktioner, der absorberer energi, ske?
 Varme artikler
Varme artikler
-
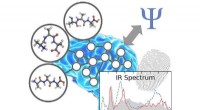 Kunstig intelligens til at opnå kemiske fingeraftrykForskerne har fundet en måde at fremskynde kemiske simuleringer ved hjælp af kunstig intelligens. Kredit:Philipp Marquetand Det er lykkedes forskere ved universiteterne i Wien og Göttingen at udvi
Kunstig intelligens til at opnå kemiske fingeraftrykForskerne har fundet en måde at fremskynde kemiske simuleringer ved hjælp af kunstig intelligens. Kredit:Philipp Marquetand Det er lykkedes forskere ved universiteterne i Wien og Göttingen at udvi -
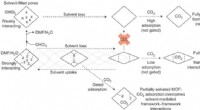 Kontinuerlig åndbar metal-organisk ramme med gæsteselektivitetForeslået rolle for gæst-ramme-interaktioner i de opløsningsmiddelafhængige kontinuerlige vejrtrækningsegenskaber af SHF-61. Kredit:(c) Naturkemi (2017). DOI:10.1038/nchem.2747 (Phys.org) —Forsk
Kontinuerlig åndbar metal-organisk ramme med gæsteselektivitetForeslået rolle for gæst-ramme-interaktioner i de opløsningsmiddelafhængige kontinuerlige vejrtrækningsegenskaber af SHF-61. Kredit:(c) Naturkemi (2017). DOI:10.1038/nchem.2747 (Phys.org) —Forsk -
 Forskere gengiver maleri i stor skala Great Wave med inkless teknologiRadical Inkless Technology producerer verdens mindste Ukiyo-e og lover at revolutionere vores udskrivning. Kredit:Kyoto University iCeMS Katsushika Hokusai (1760 - 1849) er titanen for japansk kun
Forskere gengiver maleri i stor skala Great Wave med inkless teknologiRadical Inkless Technology producerer verdens mindste Ukiyo-e og lover at revolutionere vores udskrivning. Kredit:Kyoto University iCeMS Katsushika Hokusai (1760 - 1849) er titanen for japansk kun -
 Video:Chemtrails vs. contrailsKredit:The American Chemical Society Det er let at se på det hvide spor bag et jetfly og forestille sig alle former for kemikalier, der regner ned ovenfra. Imidlertid, flyindstyr er simpelthen det
Video:Chemtrails vs. contrailsKredit:The American Chemical Society Det er let at se på det hvide spor bag et jetfly og forestille sig alle former for kemikalier, der regner ned ovenfra. Imidlertid, flyindstyr er simpelthen det
- Hvor på himlen kan måne findes?
- Hvad er affaldet skaber under respiration?
- Stenkrystaller fra dybden giver mikroskopiske spor til jordskælvs jordbevægelser
- Udtalelse:Hvorfor bioplast ikke løser vores plastikproblemer
- Værktøjer lavet af mennesker i det gamle mesopotamia
- Vilde får græssede i den sorte ørken 14, 500 år siden


